Алюмосиликаты и феррисиликаты

При выветривании авгитов образуется своеобразная глина, при чем превращение в эту глину совершается рядом последовательных этапов. Теоретически представляя себе ход глинистого выветривания авгита, нужно думать, что начало этого процесса состоит в разрушении метасиликата, количественно преобладающего. Конечный распад этого последнего должен повести к образованию углесолей кальция и магния… Читать ещё >
Алюмосиликаты и феррисиликаты (реферат, курсовая, диплом, контрольная)
Группа полевых шпатов. Мы ставим на первое место эту группу минералов как потому, что ее представители являются наиболее распространенными алюмосиликатами в большинстве почвенных типов, так и потому, что один из типов их разложения многократно изучался и ему посвящена обширная литература.
При действии воды и углекислоты, все полевые шпаты превращаются в каолин, не имеющий обычно кристаллического характера, но по своим химическим свойствам вполне идентичный с кристаллическим каолинитом. Отсутствие кристалличности в конечном продукте распада полевого шпата давало повод утверждать, что кристаллический каолинит не может быть вообще продуктом выветривания. Но и происхождение не кристаллического или неясно кристаллического каолина трактовалось различными исследователями не одинаково, при чем некоторые из них противопоставляли каолинизацию выветриванию (Штуцер, отчасти Штремме). Розлер и Вайнгиенк утверждали даже, что каолин вообще не является продуктом выветривания, а образуется, как результат послевулканического действия газов или термальных вод. Иные исследователи ставили происхождение каолина в связь с деятельностью болотных вод (Раманн, Вюст), другие отмечали случаи образования каолина под влиянием холодных углекислых источников (Гагель, Штремме).
Те исследователи, которые противополагали каолинизацию выветриванию, отмечали, что выветривание это — окислительный процесс, а каолинизация — восстановительный, что при выветривании происходит механическая дезинтеграция пород, а при каолинизации таковой не наблюдается (Штремме, Штуцер).
Изучая литературу по вопросам каолинизации, нетрудно, однако, притти к заключению, что всюду в природе, где работают вода и углекислота, откуда бы последние ни получались и какова бы ни была температура воды, они вызывают процесс коалинизации. Таким образом, каолин в природе образуется и под влиянием термальных источников и под влиянием холодных углекислых источников, и под влиянием болотных вод, и под влиянием поверхностного выветривания, а потому и не может быть одной общей теории, охватывающей генезис всех каолиновых месторождений вообще. Отметим, что в некоторых случаях возможно, повидимому, выделение каолинита и из растворов.
Если мы прибавим к сказанному, что каолин может образоваться и на земной поверхности, и на различных глубинах, куда проникают перечисленные выше природные реактивы, то будет понятно, что залежи каолина могут быть различны и по внешнему виду. Еще больше усложняет вопрос то обстоятельство, что месторождения каолинов различны по возрасту, различны по количеству времени, пошедшего на их образование, и что процесс каолинизации изучали чаще всего там, где он давно уже закончился, где каолин ясно виден, где нельзя уже наблюдать первых стадий разложения, где, следовательно, механическая дезинтеграция уже не заметна.
Достаточно отметить несомненное присутствие каолина в тропических и особенно субтропических продуктах поверхностного выветривания, чтобы не спорить о том, что каолин может образоваться путем выветривания. Здесь же можно наблюдать, что каолинизация идет параллельно с механической дезинтеграцией выветривающейся породы, что каолинизация может сопровождаться окислительными процессами, что наблюдается определенное ослабление каолинизации с глубиной и пр.
Если каолинизация идет под влиянием болотных вод или на глубинах, мало доступных кислороду воздуха, то она будет сопровождаться восстановительными процессами, при чем каолин будет освобождаться от окислов железа, в противоположность тому, что мы наблюдаем при тропическом выветривании.
Каолин или каолинит представляет свободную кремнеглиноземную кислоту (H2Al2Si208. Н20), откуда ясно, что конечная стадия распада алюмосиликатов под влиянием воды и углекислоты аналогична таковой же простых силикатов: и в том, и в другом случаях получаются свободные кислоты. Такая аналогия позволяет допустить, что и в первых фазах выветривания этих двух групп силикатов должно быть много общего, и на самом деле мы знаем, что алюмои феррисиликаты начинают свой процесс распада с поглощения небольших количеств воды, которые, изменяя свойства алюмосиликатов, вначале не разрушают их однородности. Так, Лемберг указывал на изменения физических свойств полевых шпатов при поглощении ими воды; то же говорят опыты Джонстона со слюдой, описанные выше. Дальнейшая стадия выветривания должна заключаться в отщеплении щелочей и щелочных земель и постепенном замещении их водородом, а у более кислых, богатых кремнеземом полевых шпатов и в одновременном отщеплении избыточного кремнезема, который может выпадать в виде опала и затем постепенно превращаться в кварц, а может и уноситься в растворе или псевдорастворе из продуктов выветривания. Таким образом, мы принимаем, что всякий полевой шпат, раньше чем превратиться в свободную кислоту, должен пройти ряд промежуточных стадий, в виде кислых солей, ближе пока не изученных. Повидимому, в этих случаях разрушение кристаллической сетки полевого шпата происходит уже на первых стадиях выветривания.
Уже превращение ортоклаза в слюду, принадлежащую к группе мусковита, можно рассматривать, как переход средней соли в соль кислую, хотя эта природная реакция едва ли принадлежит зоне выветривания. По данным Лакруа, такое превращение чаще всего идет в трещинах спайности, и мало-по-малу весь минерал превращается в массу пластинок бесцветной слюды, которые часто бывают скрытокристаллическими. Превращенные в слюду полевые шпаты становятся мутными, теряют свой стеклянный блеск, принимая восковой; твердость их уменьшается, а плотность возрастает. Невооруженному глазу они представляются желтыми. Это превращение часто бывает неправильным, появляясь частью в центре, частью на периферии кристалла.
Несколько образцов полуразложенных полевых шпатов исследовано Левинсоном-Лессингом, который называет процесс разложения пелитизацией в отличие от каолинизации, хотя едва ли можно сомневаться в аналогии этих двух процессов. Исследователь изучал, очевидно, первые фазы процесса, иногда, может быть, усложнявшиеся и реакциями замещения. Таковые возможны, как мы знаем из опытов Бейера, при действии слабых соляных растворов, а последние всегда принимают участие в процессах выветривания. Приведем здесь некоторые данные Левинсона-Лессинга.
Полевой шпат из порфиритоида. Пелитизирован, но есть и бесцветные участки листочков с яркой аггрегационной поляризацией. Его состав таков:
Si02 | 50,09%. |
A1203 | 29,64. |
CaO. | 14,04. |
MgO. | 1,11. |
Na20. | нет. |
H20. | 5,43. |
Продукт выветривания совершенно не содержит натрия, тем не менее считать его за вещество, подученное из анортита, нельзя, ибо в этом последнем случае продукт выветривания содержал бы меньше кремнезема. Следовательно, мы имеем здесь дело с плагиоклазом группы битовнита или лабрадора, где весь натрий выщелочен и замещен водой. Приведем затем анализы Фогта, исследовавшего лабрадор и различные стадии его выветривания. К сожалению, исследования Левинсона-Лессинга, как и исследования Фогта, не дают ясного указания, представляло ли исследованное вещество однородный продукт или смесь нескольких продуктов. Более вероятным представляется последнее предположение, но и в этом случае простой расчет показывает, что далеко не всегда в этой смеси мы можем принять присутствие неразложенного полевого шпата, каолина и кремнезема, что в иных случаях в состав смеси входят и промежуточные продукты между полевым шпатом и каолинитом — кислые алюмосиликаты.
Лабрадор свежий | Лабрадоры, отчасти каолинизированные | Более или менее чистые каолины | |||
Si02 | 54,5. | 50,03. | 49,16. | 48,61. | 47,72. |
ai2o3 | 27,0. | 28,60. | 29,60. | 29,45. | 37,40. |
Fe203 | 2,5. | 1,62. | 1,88. | 3,40. | 1,59. |
CaO. | 9,0. | 4,21. | 3,47. | 0,68. | 0,23. |
MgO. | 1,0. | 2,95. | 1,67. | 0,49. | 0,11. |
K20. | 1,0. | ок. 1,00. | —. | —. | 0,44. |
Na20. | 5,0. | ок. 1,00. | —. | —. | 0,76. |
H20. | —. | 11,90. | 13,63. | 16,38. | 11,66. |
Из цифровых данных видно, что в то время как натрий выщелочился почти нацело, извести сохранилось около половины. Отсюда, конечно, нельзя еще заключить, что альбитовая частица разрушается вообще легче, чем анортитовая, так как в той группе плагиоклазов, к которой относятся приведенные анализы, число анортитовых частиц более числа альбитовых.
Что каолинит получился из лабрадора действием воды и углекислоты, явствует из того, что иногда, хотя и редко, кальцит находится вместе с каолинитом.
При исследовании процесса выветривания в Чакве близ Батума нам удалось выделить из полуразложенной породы (авгитового андезита) продукт промежуточного распада местных полевых шпатов. Анализ этого продукта (II) приводится ниже наряду с анализом свежего полевого шпата[1]:
I. | II. | |
H20. | 0,20. | 11,21. |
Si02 | 65,49. | 57,08. |
A1203 | 20,06. | 23,32. |
Fe203 | —. | 1,08. |
CaO. | 1,58. | СЛ. |
MgO. | 0,19. | 0,42. |
K20. | 5,92. | 2,82. |
Na20. | 6,71. | 4,25. |
Реакции превращения полевых шпатов в каолин представляют обычно в таком виде.
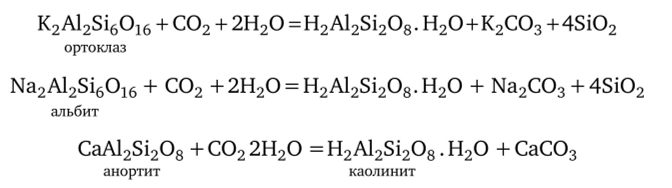
Вероятно, точнее было бы их изображать так:
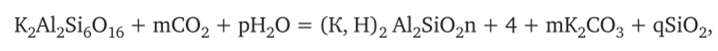
где ш, р и q могут быть и дробными, если количество частиц полевого шпата принять за единицу.
Против такого последовательного и постепенного распада полевого шпата возражал Гинзбург, но его доводы, по нашему мнению, недостаточны. Гинзбург, между прочим, упустил из виду, что в упомянутом выше продукте выветривания чаквинских полевых шпатов доказано отсутствие частиц свежего полевого шпата, а при этих условиях его нельзя трактовать иначе, как промежуточный продукт распада или смесь таковых. Эти промежуточные продукты распада своим внешним видом и некоторыми физическими свойствами гораздо ближе напоминают каолин, чем полевой шпат, откуда следует, что отличить промежуточные продукты распада простым глазом или под микроскопом, в шлифах, от каолина невозможно. Они окрашиваются фуксином так же, как каолин.
Весьма вероятно, что иногда реакция распада полевых шпатов протекает и сложнее, что, наряду с переходом в глину, часть полевого шпата растворяется в образующейся углекислой щелочи или разлагается целиком. Выше рассмотренные опытные исследования показывают нам, что глинозем, хотя и в небольших количествах, переходит из алюмосиликатов в раствор.
Группа слюд. Выветривание слюд, повидимому, происходит легче, чем выветривание ортоклаза. Лабораторные исследования показывают, что мусковит гораздо энергичнее отщепляет свою щелочь, чем ортоклаз; о том же свидетельствуют культурные опыты Вотчала и Прянишникова[2], согласно которым растения гораздо успешнее развиваются, если калийные соли доставляются в виде мусковита, чем в том случае, когда источником калия является ортоклаз. Аналогичные результаты получил Самойлов, культивируя гриб Aspergillus niger. Особенно легко разлагаются черные слюды (группа биотита). Во всякой поверхностной породе, содержащей биотит, происходит весьма заметное на глаз изменение слюды, носящее название выцветания. По исследованиям Цшиммера, выцветание обусловливается прежде всего выделением Fe203 (в виде гидрата). Наряду с этим выделением идет потеря калия и замещение его водородом. Конечным продуктом выветривания мусковита, состав которого может быть определен формулой (К, Н)2 Al2Si208, является каолинит. Продукты выветривания биотитовых слюд, состав которых выражается формулой (К, Н)2(А1, Fe)2Si208. (Mg, Fe)2Si04, насколько удалось выяснить до сих пор, разнообразны. Мы знаем, в настоящее время несколько типов распада, а именно:
1. Выцветание, которое заканчивается образованием из биотита, каолинита. Обычно такой каолинит сохраняет внешнюю форму произведшего его биотита и некоторые свойства биотита. При этой реакции происходит образование вторичного кварца, являющегося, главным образом, продуктом конечного распада оливинового ядра биотита. Обычно в каолините, полученном из биотита, сохраняется небольшое количество окиси железа, большая же часть феррисиликата, входящего в состав биотита, разлагается. Выщветание — весьма распространенный в природе тип выветривания биотита. Его факторами являются вода и углекислота. Органические вещества, повидимому, играют роль лишь постольку, поскольку они способствуют выносу из продукта выветривания железа, получившегося при распаде феррисиликата. Титановая кислота, не представляющая редкости в составе биотита, выделяется при этом процессе в виде тонких игл рутила. Иногда образуется и промежуточная стадия в форме включений ильменита (титанистого железняка).
Постепенную каолинизацию биотита нам удалось проследить на образцах этого минерала из Бедой Церкви (Киевского округа). В ниже приводимой таблице сообщаем аналитические данные для последовательных продуктов выцветания биотита.
Свежий биотит. Уд. в. 3,11. | Темный золотистый биотит. Уд. в. 2,83. | Серебристый биотит. Уд. в. 2,80. | Белые пластинки с еле заметным зеленоват, оттенком. | |
н2о. | 2,37. | 5,05. | 5,44. | 12,76. |
Si02 | 36,63. | 34,71. | 40,93. | 43,36. |
Ti02 | 1,28. | 3,19. | 0,46. | —. |
ai2o3 | 17,37. | 15,46. | 19,43. | 34,31. |
Fe203 | 6,75. | 12,56. | 8,92. | 3,98. |
FeO. | 15,41. | 2,80. | 1,94. | —. |
МпО. | 1,04. | 0,80. | —. | —. |
MgO. | 9,73. | 15,77. | 13,80. | 2,43. |
СаО. | 0,23. | 1,89. | 0,50. | —. |
К20. | 8,15. | 7,32. | 7,52. | 2,67. |
Na20. | 0,94. | 0,68. | 0,87. | 0,33. |
Сумма. | 99,90. | 100,2. | 99,81. | 99,84. |
Конечные стадии того же процесса нам удалось разыскать среди выветривающихся биотитов Искорости (по жел. дор. Киев — Ковель) и с. Хажйна б. Бердичевского у. Эти стадии являются в виде белых пластинок и обломков кристаллов с шелковистым блеском и ясно выраженной спайностью. Их состав приводится непосредственно ниже:
Псевдоморфозы каолинита по биотиту. | ||
Искорость. | Хажин. | |
н2о. | 14,11. | 15,43. |
Si02 | 46,33. | 44,76. |
Ti02 | —. | 1,14. |
Окончание таблицы
Псевдоморфозы каолинита по биотиту. | ||
Искорость. | Хажин. | |
А1203 | 37,40. | 36,61. |
Ре23. | 2,03. | 2,04. |
СаО. | 0,07. | Сл. |
MgO. | 0,13. | 0,06. |
100,07. | 100,04. | |
2. Выветривание биотита с сохранением феррисиликата. Этот тип распада представляется довольно редким и найден был нами в нижних горизонтах полуболотных почв Белой Церкви. Получающийся при этом типе распада зеленый порошкообразный продукт, при исследовании под микроскопом, оказывается состоящим из мелких двупреломляющих листочков; он залегает обыкновенно внутри плотных комков. Его образование связано, повидимому, с условиями слабой аэрации почвы, что в болотных образованиях обычно.
Особенной прочностью зеленый порошкообразный продукт не отличается и, при благоприятных условиях, также каолинизируется. Процесс превращения биотита в зеленое порошкообразное вещество и дальнейшей каолинизации этого последнего представлен в нижеследующей таблице:
Серебрист. биотит. | Ярко; зелен. порошок. | Грязнозелен. порошок. | Слабо-зелен, каолиноподоб. масса. | Белая каолиноподоб. масса. | |
Н20. | 5,44. | 9,24. | 10,88. | 11,25. | 12,77. |
Si02 | 40,93. | 48,67. | 48,82. | 47,76. | 46,20. |
ТЮ2 | 0,46. | 0,20. | 0,21. | —. | —. |
А12о3 | 19,43. | 23,60. | 23,77. | 34,47. | 37,28. |
Fe303 | 8,92. | 10,03. | 9,89. | 2,62. | 1,44. |
FeO. | 1,94. | 1,57. | 0,76. | —. | |
MgO. | 13,80. | 3,01. | 2,73. | 1,86. | 0,64. |
СаО. | 0,50. | сл. | СЛ. | —. | —. |
к3о. | 7,52. | 2,92. | 2,60. | 1,94. | 1,28. |
Na20. | 0,87. | 0,31. | 0,28. | 0,24. | 0,21. |
Сумма. | 99,81. | 99,94. | 99,95. | 100,14. | 99,82. |
3. Среди выветривающегося биотита Белой Церкви были найдены голубовато-зеленые листки, состав которых таков:
Н20. | 9,62. |
Si02 | 35,68. |
А12о3 | 18,76. |
Fe203 | 4,91. |
FeO. | 6,54. |
MgO. | 20,29. |
MnO. | 1,78. |
К20. | 2,40. |
Na20. | 0,10. |
Повидимому, это также продукт изменения биотита, но получился ли он при процессах выветривания, или представляет продукт более раннего метаморфоза, неясно. Повидимому, в его образовании принимали участие растворы магнезиальных солей.
Особенно богатые окисью железа слюды (лепидомелан), повидимому, выделяют все железо в виде гидрата окиси. Аналогично со слюдами выветривается глауконит.
Группа нефелина (нефелин, содалит, гаюнин, нозеан и др.). Возможность превращения нефелина в калийную слюду, доказанная опытным путем (Тугут), и такое же превращение его, наблюдавшееся в природе (Бишоф), приводят к выводу, что конечным продуктом выветривания этого минерала, при действии воды и углекислоты, является каолиновая глина. Для нозеана и гаюина наблюдались в природе переходы в каолин (Fritsch, Seilern). Других типов распада, повидимому, не отмечалось.
Лейцит. Хотя составу этого минерала (K2Al2Si4012) отвечает свободная кислота H2Al2Si4012 (пирофиллит), однако, перехода лейцита в эту именно кислоту не наблюдалось. Как и кислые полевые шпаты, лейцит, отщепляя избыток кремнезема и щелочь, постепенно превращается в каолиновую глину; согласно Блюму, процесс начинается с поверхности и распространяется в глубину. Кристаллы первоначально становятся матовыми, непрозрачными и покрываются белой тонкозернистой коркой. Кристаллы сохраняют свою форму вплоть до полного разложения[3].
Группа граната. Минералы этой группы особенной распространенностью в почве не отличаются, однако, во всех почвах Сев. Европы, образовавшихся из ледниковых наносов, присутствуют в небольших количествах. Обычно встречается альмандин. Представляя, как и магнезиальные слюды, продукты присоединения к алюмосиликатному (слюдяному) ядру ортосиликатной группы (R2Al2Si208. R2Si04), они должны отличаться и сходными типами превращений. Легче других выветривается, повидимому, гроссуляр (CaAl2Si208. Ca2Si04), труднее — альмандин (Mg, Fe) Al2Si208. (Mg, Fe)2Si04 и пироп (MgAl2Si208. Mg2Si04). При выветривании гранаты переходят в глины каолинового типа.
Так же выветриваются и минералы группы эпидота [3 (CaAl2Si208). Са (НО)2]. По мнению акад. Вернадского, минералы группы мелилита представляются изомерами гранатов. Они являются продуктами присоединения алюмоили феррисиликатов к оливиновому ядру, т. е. их состав может быть выражен формулой pR2 Si04. qRAl2Si208. В частности, мелилит имеет состав pCa2Si04. qCaAl2Si208. Эти минералы, при выветривании, глин не дают, а превращаются в конечном итоге в опалы, образуя, в качестве промежуточных продуктов, силикаты, богатые гидроксильными группами, т. е. кислые силикаты.
Группа глиноземсодержащих пироксенов и амфиболов. Наиболее распространенные минералы этой группы представляют изоморфные смеси, в которых роль растворителя играет метасиликат (RSi03); в нем растворены два алюмо- (ферри-) силиката: так называемый силикат Чермака (хлористое ядро) — RAl2Si06 и эгириновый силикат — R2(Fe, Al)2Si4012. В природе выветривание авгитов (пироксенов) происходит энергичнее, чем выветривание роговых обманок (амфиболов), что, быть может, находится в зависимости от различия в величине частицы этих двух минеральных групп.
При выветривании авгитов образуется своеобразная глина, при чем превращение в эту глину совершается рядом последовательных этапов. Теоретически представляя себе ход глинистого выветривания авгита, нужно думать, что начало этого процесса состоит в разрушении метасиликата, количественно преобладающего. Конечный распад этого последнего должен повести к образованию углесолей кальция и магния, выделению гидратов окиси железа и выносу кремнезема. Эти теоретические соображения подтверждаются наблюдениями в природе. В пример промежуточого продукта выветривания авгита можно привести изученный нами образец из Фрисарки Волынской губ. (Глинка К.). Орбазец взят из глубоких горизонтов выветривания, куда органические кислотьп гумуса проникают в ничтожных количествах. Полуразложенный авгит сохраняет кристалличность, но становится мягким, глинообразным; его окраска грязновато-зеленая. Состав этого промежуточного продукта выражается следующими данными:
Н20. | 8,38%. |
Si02 | 51,36. |
А1203 | 18,97. |
Ре203 | 13,27. |
FeO. | 1,71. |
СаО. | 3,27. |
MgO. | 2,34. |
99,30%. |
Полное превращение авгита в глину с разрушением всего метасиликата и с выпадением из раствора изоморфной смеси хлоритоидного и эгиринового ядер, при чем металлы этих ядер замещены водородом, можно наблюдать в Чакве близ Батума, где находятся, между прочим, псевдоморфозы глинистого вещества по авгиту (Глинка, К.). Состав этого глинистого вещества, имеющий ясное кристаллическое строение, определяется следующими данными:
Н20 при прокал. | 14,63%. |
Si02 | 50,08. |
А1203 | 28,97. |
Ре203*. | 5,60. |
MgO. | 0,64. |
* Часть Fe203 принадлежит, повидимому, лимониту.
Минерал напоминает своим составом так называемый анауксит, глинистое вещество, слагающее псевдоморфозы по авгиту в Билине (Богемия). До последнего времени не было, однако, анализов вполне чистого билинского анауксита, который как и чаквинский, ясно кристалличен. Наиболее точным в этом смысле может считаться анализ фон-Гауэра, цифры которого все же значительно отличаются от цифр В. Смирнова, исследовавшего позже чистый кристаллический билинский анауксит. Приводим параллельно анализы обоих исследователей1:
Ф. Гауэр | В. Смирнов. | |
н2о. | 10,58%. | 12,64%. |
Si02 | 56,50. | 50,75. |
А1203 | 26,06. | 33,34. |
Ре203 | 5,44. | 2,45. |
СаО. | 0,90. | 0,32. |
MgO. | 0,58. | 0,27. |
Наряду с ясно кристаллическим анаукситом из авгита получается и не кристаллическая глина, близкая по составу к анаукситу, называемая цимолитом.
Аналогичные с авгитовыми промежуточные продукты выветривания роговой обманки анализированы Лембергом из эклогита.
I. | II. | |
н2о. | 1,77%. | 10,44%. |
Si02 | 52,23. | 37,82. |
А1203 | 4,52. | 11,50. |
Ре203 | 4,08. | 7,10. |
MgO. | 18,30. | 29,34. |
СаО. | 19,10. | 8,39. |
1 По вопросу о выветривании авгитов см. также Кпор и Lemberg.
Группа цеолитов. Для изучения типов выветривания этих богатых водою алюмосиликатов мы располагаем целым рядом данных, полученных частью при исследовании процессов выветривания среди красноземов Чаквы, частью при изучении тех же процессов среди подзолистых почв горы Цхра-Цкаро на Кавказе (Глинка К.).
1-й тип. При выветривании цеолитов (томсонита или сколецита) среди краснозема Чаквы происходит превращение последних в глину, отличающуюся от каолиновой; к этой глине примешивается небольшое количество свободного гидрата глинозема. Состав продукта выветривания таков:
Н20 при 100° Ц. | 15,87%. |
Н20 «прокал. | 11,12. |
Si02 | 37,65. |
ai2o3 | 34,53. |
СаО. | 0,56. |
В массе этой глины, в виде тонких белых жил, прорезающих местами красную массу чаквинских продуктов выветривания, сохранились кое-где кристаллические сростки белого цвета, лишь с поверхности иногда подернутые пленкой гидрата окиси железа. Состав этих кристаллов таков:
Н20 при 100° Ц. | 13,98%. |
Н20 «прокал. | 15,79. |
Si02 | 35,40. |
ai2o3 | 29,30. |
СаО. | 4,22. |
Na20. | 1,15. |
Из аналитических данных получается формула (Н2, Na2, Са) Al2Si208. 5Н20, из которой видно, что минерал представляет кислый алюмосиликат, одну из промежуточных стадий превращения цеолита в глину. Этот кислый алюмосиликат разлагается соляной кислотой так же легко, как произведший его цеолит, но отличается от последнего значительно меньшей твердостью и отсутствием плавкости.
2-й тип, наблюдавшийся на Цхра-Цкаро, близок к предыдущему в том смысле, что и здесь мы наблюдаем переход средней соли в соль кислую, но есть и некоторая разница. Выветриванию подвергался радиально-лучистый натролит (галактит), который, постепенно расщепляясь на тонкие волокна, превратился, в конце концов, в мякинообразную массу, сложенную из перепутанных тонких кристалликов-волоконец. Состав натролита (I) и продукта его выветривания (II) представлен в нижеследующей таблице[4]:
I. | II. | |
Н20. | 10,57. | 15,50. |
Si02 | 47,01. | 44,16. |
А1203 | 27,93. | 28,60. |
Fe203 | Сл. | 2,12. |
СаО. | 2,48. | 7,45. |
Na20. | 12,21. | 2,05. |
Очевидно, что, наряду с замещением части натрия водородом, другая его часть замещается кальцием. Одновременно происходит и замещение глинозема железом. Понятно, такого рода реакции не могли произойти при действии только воды и углекислоты; вероятнее всего, что, наряду с последними, действовали и вещества гумуса.
3-й тип наблюдался также у цеолитов Цхра-Цкаро, добытых из подзолистых горизонтов местных почв. Плотный цеолит, расщепляясь на отдельные волоконца, превращается, в конце концов, в вату, состоящую из тончайших иголочек. Химический состав плотного цеолита (I) и полученного из него продукта распада (II) приводится в таблице:
I. | II. | |
Н20. | 13,05%. | 13,64%. |
Si02 | 42,44. | 47,42. |
А1203 | 28,87. | 25,23. |
Fe203 | —. | 1,07. |
СаО. | 11,81. | 8,95. |
Na20. | 3,60. | 3,52. |
Из сопоставления аналитических данных видно, что выветривание лишило цеолит части оснований и глинозема, увеличив процентное содержание кремнезема. Количество воды осталось почти без перемены. Короче говоря, распад цеолита совершается таким образом, как если бы на него действовала кислота более энергичная, чем угольная и ей подобные. В виду условий залегания цеолита становится вероятным предположение, что он выветривался под влиянием более подвижных и энергичных кислот гумуса.
Задумываясь над фактами, касающимися выветривания в природе алюмосиликатов, мы приходим к заключению, что выветривание одного и того же минерала может направиться различными путями, в зависимости от условий, при которых совершается процесс выветривания. Следовательно, не только разложение органических веществ приводит в природе к неодинаковым комплексам гумуса, но и распад минералов дает неодинаковые продукты выветривания. Иначе говоря, весь процесс почвообразования целиком должен быть неодинаков при различных природных условиях, и каждая определенная комбинация этих условий должна дать и определенный процесс, а значит, и определенный почвенный тип.
Чтобы закончить с выветриванием отдельных минералов, нам остается еще рассмотреть превращение солей галоидных и других кислот, каковы фосфорная, серная, угольная и проч. В большинстве случаев здесь процессы много проще и яснее, так как большая часть этих соединений растворима в воде. Таким образом, выветривание чаще всего заключается в растворении и выносе этих минералов из выветривающейся породы. Наблюдаются, впрочем, иногда и другие процессы: окисление, гидратация, восстановление и пр.
Фосфорнокислые соли. Из последних особенно интересны превращения вивианита [Fe3(P04)2. 8Н20], подробно изученные С. Поповым на Керченском полуострове. Встречающийся здесь вивианит, как видно из приводимого ниже анализа, не представляет чистой железной соли; часть закиси железа здесь замещена магнезией, известью и окисью марганца. Минерал имеет формулу (Fe, Mn, Mg, Са)3 (Р04)2. 8Н20 и получил от исследователя название паравивианита.
р2о5 | 27,01. | |
FeO. | 39,12]. | 43,53. |
МпО. | 2,01. | |
MgO. | 1,92. | |
СаО. | 0,481. | |
н2о. | 28,75. | |
При выветривании происходит постепенное окисление железа, при чем минерал остается кристаллическим, пока все закисное железо не перейдет в окисное. Поповым изучены следующие стадии превращений:

Карбонаты. При нормальном давлении и средних температурах, т. е. при тех условиях, которые существуют на земной поверхности, карбонаты отличаются следующей растворимостью:
в 10.000 част, углекислой воды: | |
СаС03 | 10 ч. |
MgC03 | 13,1 «> |
FeC03 | 7,2″. |
MnC03 | 4—5 «. |
Впрочем, растворимость природного углекислого кальция может меняться в зависимости от того, встречается ли он в виде кальцита, арагонита или люблинита. Растворимость карбонатов, как и других солей, сильно изменяется в зависимости от состава и температуры действующих на них почвенных растворов[5].
Две последние соли на земной поверхности неустойчивы: первая из них при действии воды и кислорода воздуха, переходит в один из гидратов окиси железа, чаще всего в лимонит, вторая превращается в пиролюзит или гидраты окиси марганца.
Сульфаты. В 10.000 ч. воды растворяется в среднем около 20 ч. ангидрида и 25 ч. гипса. В углекислой воде растворимость не повышается, но повышается в присутствии NaCl и Na2S04. Барит (BaS04) требует для растворения одной части 40.000 частей воды (Фрезениус); азотнокислый аммоний повышает растворимость.
Некоторые сернокислые соли способны поглощать воду: так, например, ангидрид в природе очень часто переходит в гипс. Некоторые соли закисей металлов, в присутствии воды и кислорода воздуха, переходят в окисные соли, например, железный купорос (FeS04. 7Н20). Наконец, в присутствии органических веществ и при содействии микробиологических процессов сернокислые соли восстановляются, переходя в сернистые соединения. Последние, в присутствии воды и углекислоты, дают карбонаты и H2S. Из группы сульфатов в продуктах выветривания особенно распространены гипс и глауберова соль, реже встречаются сернокислые соли магния, например, эпсомит (MgS04. 7 Н20). Сульфаты железа, глинозема встречаются обычно там, где выветриваются пирит и марказит. Образование сульфатов железа и алюминия следует также допустить в условиях последовательной смены процессов восстановления окислительными процессами (болотные почвы).
Галоидные соли. Из этой группы особенно распространены в продуктах выветривания хлористые соли, а из последних — NaCl. Встречаются, хотя и значительно реже, КС1, MgCl2 и даже СаС12. Высокая растворимость хлористых солей обусловливает то обстоятельство, что в почвах они встречаются в особо благоприятных случаях. О бромистых и йодистых солях можно не упоминать, фтористые же могут встречаться в качестве остатков первичных минералов (напр., плавиковый шпат).
Азотнокислые соли присутствуют в небольших количествах во всех почти почвах, но накопляться, в виду их легкой растворимости, могут лишь в исключительных случаях (сухие, бездождные области).
- [1] О выветривании полевых шпатов см. Bischoff, Struve, Gehlen, Fuchs, Forchhammer, Fournet, Malaguti, Crass o, Suckow, Roth. О каолинизации лабрадоров, в частности, кромеФогта см. Rose, Delesse, Лаврский, Самойлов, Kossmann. Bericht iiber die Thatigkeit dernaturw. Section der Schles. Ger. im Jahr 1885.
- [2] Дневник XI съезда русск. естествоисп. и врачей.
- [3] О каолинизации лейцита см. также Rammeisberg.
- [4] О выветривании натролита см. также Cornu F. u. Schuster С.
- [5] По отношению к карбонатам см. Cameron F. and Bell J., U. S. Depart, of Agricult., Bureau of soils, Bull. № 49.