Вольтамперометрический метод анализа

Рис. 4.28. Вольтамперограммы, полученные на стационарном (а) и вращающемся (6) твердом электроде Инверсионную вольтамперометрию применяют для определения крайне низких концентраций веществ, вплоть до 10−9 М. Существует несколько вариантов метода. Во всех вариантах первой стадией процесса является предварительное электрохимическое концентрирование определенных веществ, что приводит к существенному… Читать ещё >
Вольтамперометрический метод анализа (реферат, курсовая, диплом, контрольная)
Вольтамперометрия — электрохимический метод анализа, основанный на изучении зависимости тока, протекающего через электролитическую ячейку, от напряжения. Она является качественным и количественным методом анализа.
Вольтамперометрия — высокочувствительный и экспрессный метод определения неорганических и органических веществ, пригодный для анализа химических, геохимических, биохимических, медицинских, фармацевтических и других объектов. Это один из наиболее универсальных методов определения следовых количеств веществ, он позволяет одновременного определять несколько компонентов (в оптимальных условиях эксперимента — до четырех-пяти), а также имеет линейную зависимость тока от концентрации в диапазоне 10-8—10~2 М.
Первым из многочисленных вольтамперометрических методов был метод полярографии, который в 1922 г. разработал Я. Гейровский (J. Heyrovsky — чешский химик, 1890—1967). Суть метода состоит в том, что используют постоянно обновляющийся электрод (ртутную каплю) и снимают зависимость тока от напряжения.
По решению Международного союза по теоретической и прикладной химии (IUPAC) термин «вольтамперометрия» было решено использовать в качестве обобщающего, а термин «полярография» сохранить только для частного случая — применения ртутного электрода с обновляемой поверхностью.
Полярография. Рассмотрим принцип полярографии для случая, когда в растворе находятся ионы металлов, которые электролитически восстанавливаются на ртутном катоде. В этот раствор (рис. 4.23, а) опускают два электрода. Один — капля ртути (катод), периодически вытекающая из капилляра, такой электрод называют капающим ртутным. Другой — слой ртути с большой поверхностью на дне ячейки (анод). Электроды соединяют с источником постоянного тока и постепенно повышают напряжение Е со скоростью 2—5 мВ/e, фиксируя изменение силы тока I.
Для обеспечения достаточно высокой электропроводности в ячейку добавляют 0,05—1 М раствор индифферентного электролита (фона). Обычно можно пренебречь током, протекающим через двойной слой ячейки, поэтому.

Это означает, что вид подпрограммы определяется только величиной сопротивления капающего ртутного электрода R.m.
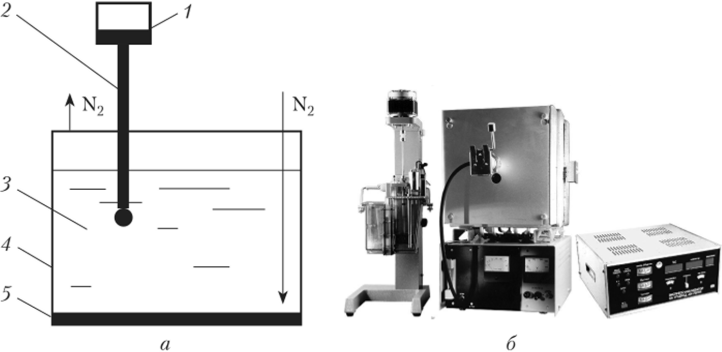
Рис. 4.23. Полярограф:
а — полярографическая ячейка: 1 — сосуд с ртутью; 2 — капилляр;
3 — анализируемый раствор; 4 — корпус ячейки; 5 — донная ртуть (анод); б — внешний вид универсального полярографа Капающий ртутный электрод обладает следующими качествами:
- • строгое чередование зарождения, роста и отрыва капель обеспечивают хорошую воспроизводимость площади поверхности и постоянное ее обновление, поэтому воспроизводимость подпрограмм практически абсолютная;
- • электрод является почти идеально поляризуемым в очень широком интервале потенциалов, ограниченном в анодной области электродными реакциями окисления ртути (+0,4 В в кислой и 0,006 В в щелочной среде), а в катодной — реакциями восстановления иона Н+ (от -1 до -1,5 В в зависимости от концентрации кислоты) или катиона фонового электролита (от -2 В для ионов щелочных металлов до -2,5 В для R/, N+). Это позволяет изучать и определять вещества, восстанавливающиеся при очень высоких отрицательных потенциалах, что невозможно на электродах из иных материалов;
- • многие металлы после своего восстановления образуют амальгамы, т. е. накапливаются в ртути, а не остаются на ее поверхности.
При проведении полярографического анализа требуется соблюдение следующих условий:
- • для поддержания необходимой УЭП анализируемого раствора в него вводят фоновый электролит, например хлорид или нитрат калия, хлорид аммония и др. Концентрация фонового электролита должна быть выше концентрации полярографически активного вещества в оптимальном случае не менее чем в 100 раз. При этом концентрация самого полярографически активного вещества обычно лежит в пределах от 10-5 до 102 моль/л;
- • необходимо термостатировать полярографическую ячейку, поддерживая температуру постоянной с погрешностью ±0,5°С;
- • перед проведением полярографического анализа из анализируемого раствора удаляют растворенный в нем кислород, для чего пропускают инертный газ (азот) в течение 15 мин.
Схема полярографической установки для регистрации подпрограмм показана на рис. 4.24. Электролитическую ячейку ЭЯ включают в цепь, состоящую из источника постоянного напряжения Е, калиброванного сопротивления АБ, вольтметра V и устройства для регистрации тока Г. Перемещая движок С вдоль реостата АБ, на электролитическую ячейку подают напряжение от внешнего источника Е и регистрируют протекающий через нее ток.
Раздельные волны на полярограмме получаются при АЕи2 >0,1 В, если концентрации компонентов смеси равны. При других соотношениях концентраций необходима еще большая разность потенциалов полуволн. Род вещества соответствует напряжению полуволны ?½, а его концентрация — высоте волны Д/.
Классическая полярограмма в идеализированном виде изображена на рис. 4.25. Ее характеристиками являются: сила предельного диффузионного тока ID, мкА (или пропорциональная величина — высота волны, мм), потенциал в точке максимального наклона участка Б—В (I = ID/2), называемой потенциалом полуволны Е{/2, В, и наклон восходящего участка Б—В.
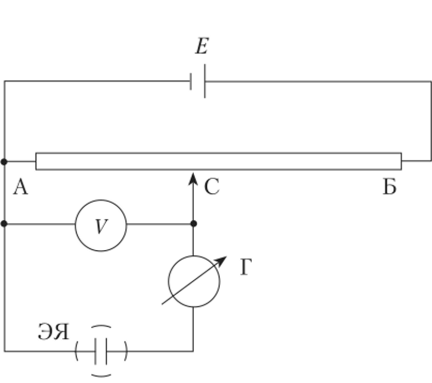
Рис. 4.24. Схема полярографической установки:
ЭЯ — электролитическая ячейка; Е — источник постоянного напряжения; АБ — калиброванное сопротивление; С — движок; V — вольтметр;
Г — устройство для регистрации тока.
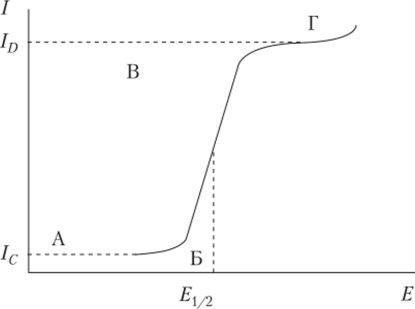
Рис. 4.25. Классическая подпрограмма:
1С — остаточный ток; ID — диффузионный ток Как следует из рис. 4.25, подпрограмма состоит из трех участков: пологого А—Б, Б—В, характеризующегося резким подъемом тока за счет электрохимической реакции, и, наконец, Б—Г, соответствующего установлению практически постоянного значения тока. Подъем тока в точке Г обусловлен новой электрохимической реакцией. Рассмотрим каждый из этих участков подробнее.
На начальном участке А—Б ток с изменением потенциала меняется очень слабо. Это означает, что до начала электрохимической реакции (точка Б) ртутный электрод является почти идеально поляризуемым. Небольшой ток, протекающий на начальном участке подпрограммы, называют остаточным. Основной вклад в него вносит формирование двойного электрического слоя — конденсатора (см. параграф 4.1).
Поверхность ртути, как любого металла, в растворе заряжена. При разомкнутой цепи ртуть заряжена положительно. При увеличении потенциала положительный заряд уменьшается, достигает нуля (точка нулевого заряда) при потенциале, зависящем от природы аниона фона, и затем ртуть заряжается отрицательно. Это выражается так называемой электрокапиллярной кривой. Заряд образующегося молекулярного конденсатора q определяется соотношением.

где q — заряд; Е — потенциал; С — емкость конденсатора.
Расстояние между «пластинами» (одна — поверхность ртутного капельного электрода, другая — плоскость, проходящая через центры ближайших к нему ионов) составляет порядка 0,1 нм, поэтому емкость конденсатора достаточно велика.
Процесс формирования и заряжения конденсатора повторяется на каждой капле, поэтому протекает небольшой, но устойчивый ток заряжения (емкостный ток 1С)

С учетом изменения поверхности капли S имеем.
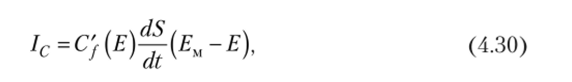
где Ем — точка нулевого заряда; C’j (E) — емкость, отнесенная к единице поверхности.
Вторым слагаемым остаточного тока является ток, обусловленный восстановлением электроактивных примесей, чаще всего плохо удаленного кислорода. Остаточный ток не связан с концентрацией определяемого вещества, поэтому его желательно уменьшить. Вклад, вносимый электроактивными примесями, снижают, применяя чистые реактивы и воду. Однако ток заряжения 1С в условиях классической полярографии снизить нельзя, и это ограничивает ее возможности.
При достижении точки Б (потенциал выделения) начинается электрохимическая реакция. С этого момента рост тока опережает рост потенциала электрода — электрод деполяризуется. Поэтому вещество, участвующее в электрохимической реакции, называют деполяризатором.
В итоге предельный ток определяется только диффузией деполяризатора из объема раствора в обедненный приэлектродный слой, поэтому его называет диффузионным, 1п. Он пропорционален концентрации деполяризатора в растворе С (уравнение Ильковича).


где п — число электронов, принимающих участие в электродной окислительно-восстановительной реакции; D — коэффициент диффузии восстанавливающего вещества; т — масса ртути, вытекающей из капилляра в секунду; т — время образования капли ртути при потенциале полуволны (3—5 с).
Масса ртути т и время каплеобразования т зависят от характеристик ртутного капающего электрода и высоты столбика ртути.
Стеклянный капилляр ртутного капающего микроэлектрода обычно имеет внешний диаметр 3—7 мм, внутренний — 0,03—0,05 мм, длину — 6—15 см. Высота ртутного столбика от нижнего конца капилляра до верхнего уровня поверхности ртути в резервуаре обычно составляет 40—80 см.
Уравнения (4.28)—(4.32) справедливы для классической полярографии, когда скорость развертки потенциала не превышает 2—5 мВ/e и электродный процесс обусловлен только диффузией и протекает обратимо.
Ток, протекающий через ячейку, является суммой фарадеевского (аналитический, полезный сигнал) /ф и емкостного (помеха) 1С токов.
Соотношение /ф//с можно улучшить за счет увеличения /ф, уменьшения /с и, наконец, разделения /ф и 1С. Эти возможности реализуются в осциллографической полярографии и инверсионной вольтамперометрии (увеличение /ф), импульсной и квадратно-волновой переменнотоковой полярографии (уменьшение /с) и полярографии на синусоидальном переменном токе (разделение /фИ/С).
Если в анализируемом растворе присутствует несколько восстанавливающихся веществ, причем разность между значениями их потенциалов полуволны составляет не менее 0,2 В, то на полярограмме наблюдается несколько волн, каждая из которых отвечает тому или иному восстанавливающемуся веществу (интегральная, классическая полярограмма — рис. 4.26, а, дифференциальная полярограмма — рис. 4.26, б). Уже при разности потенциалов пиков порядка 0,02—0,05 В на дифференциальной полярограмме можно наблюдать раздельные пики вместо суммарной волны на интегральной полярограмме. Поэтому она более чувствительная, чем интегральная.
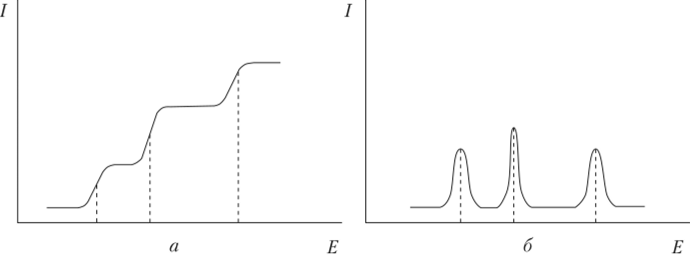
Рис. 4.26. Классическая полярограмма трех веществ:
а — интегральная; б — дифференциальная Значения потенциала полуволны ?½ некоторых катионов металлов (относительно потенциала насыщенного каломельного электрода) приведены в табл. 4.1.
Таблица 4.1
Значения потенциала полуволны Eij2 некоторых металлов
Электродная реакция. | Ex/2y В. | Фоновый электролит (состав фона). |
As3+ + Зе = As. | — 0,7. | 1 моль/л H2S04 + 0,01% желатина. |
Cd2+ + 2е = Cd. | — 0,60. | 0,1 моль/л НС1. |
Cd2+ + 2е = Cd. | — 0,79. | 6 моль/л НС1. |
Со2+ + 2е = Со. | — 1,03. | 1 моль/л KSCN. |
Си2+ + 2е = Си. | 0,5 моль/л H2S04 + 0,01% желатина. | |
Си2+ + 2с = Си. | — 0,38. | 1 моль/л Na2C4H4Oe, pH = 12. |
Fe2+ + 2е = Fe. | — 1,37. | 1 моль/л НСЮ4, pH = 0−2. |
Мп2+ + 2с = Мп. | — 1,54. | 0,5 моль/л NH3 + 0,5 моль/л NH4C1. |
Ni2+ + 2е = Ni. | — 1Д. | НСЮ4, pH = 0−2, 1 моль/л КС1. |
Ni2+ + 2е = Ni. | — 1,06. | 1 моль/л N1I3 + 0,2 моль/л NII4C1 + 0,005% желатина. |
Zn2+ + 2е = Zn. | — 1,02. | 1 моль/л КС1. |
Zn2— + 2e = Zn. | — 1,33. | 1 моль/л NH3 + 0,2 моль/л NH4C1 + 0,005% желатина. |
Zn2+ + 2e = Zn. | — 1,49. | 1 моль/л NaOH. |
Развитие классической полярографии привело к созданию следующих методов.
Осциллографическая полярография. В этом методе, в отличие от классической полярографии, изменение внешнего налагаемого на ячейку напряжения происходит очень быстро. Если в классической полярографии работают со скоростями развертки потенциала 0,1—0,4 В/мин, то в осциллографической полярографии скорость развертки составляет 0,1—2 В/с, запись вольтамперной кривой продолжается около 1 мин. Это и обуславливает особенности метода и позволяет улучшить его характеристики, т. е. чувствительность и разрешающую способность.
Для измерения тока применяют либо осциллограф, либо другое устройство, позволяющее фиксировать быстрое изменение тока.
Метод дает возможность определять более низкие концентрации веществ, чем эго позволяет классическая полярография.
Импульсная полярография. Поляризующее напряжение можно подавать на электрод не непрерывно, но линейному закону, как в классической и осциллографической полярографии, а отдельными кратковременными импульсами.
В нормальной импульсной полярографии на индикаторный электрод подают линейно увеличивающиеся импульсы напряжения, наложенного на постоянный начальный потенциал. Каждый импульс подают на новую каплю, и через 50 мс потенциал возвращается к исходной величине. Нормальная импульсная полярограмма имеет ту же форму, что и классическая.
В дифференциальной импульсной полярографии на линейно увеличивающееся постоянное напряжение (5 мВ/e) через равные промежутки времени подают одинаковые (20—100 мВ) добавочные импульсы в течение примерно 20 мс.
Переменно-токовая полярография. С помощью этого метода на электроды одновременно с линейно возрастающим постоянным напряжением Еп подают синусоидальное переменное напряжение с фиксированной частотой (-50 Гц) и небольшой амплитудой (ДЕ = 10 мВ):

Известны две разновидности переменно-токовой полярогографии — синусоидальная и квадратно-волновая. В методе синусоидальной переменно-токовой полярографии поляризующее напряжение является суммой линейно увеличивающегося постоянного напряжения Еп и переменного синусоидального напряжения частотой 50 Гц и амплитудой 10 мВ. В методе квадратно-волновой переменно-токовой полярографии линейно изменяющееся постоянное напряжение модулируют прямоугольными импульсами переменного напряжения.
Вольтамперометрия — это электрохимический метод, основанный на изучении вольтамперограмм, полученных с любым индикаторным электродом (вращающимся или стационарным, платиновым или графитовым, стационарным или статическим ртутным), кроме капающего ртутного. Различают прямые, косвенные (амперометрическое титрование) и инверсионные вольтамперометрические методы.
Индикаторным электродом обычно служит вращающийся платиновый или микроэлектрод из графита, пирографита или стеклоуглерода. В инверсионной вольтамперометрии применяют также стационарный ртутный электрод (висящая ртутная капля) и пленочные ртутные электроды на подложке из стеклоуглерода.
Индикаторные электроды из платины или графита отличаются от капающего ртутного электрода, во-первых, гем, что они имеют другой интервал поляризации, и, во-вторых, что их поверхность во время регистрации вольтамперограммы не возобновляется.
Платиновый и графитовый электроды пригодны до потенциалов +(1,4— 1,6) В. При более высоких положительных потенциалах на электроде протекает реакция с участием растворенного кислорода.
Для регистрации вольтамперограмм применяют двухи трехэлектродные ячейки (рис. 4.27).
Двухэлектродная ячейка состоит из индикаторного электрода и электрода сравнения (рис. 4.27, а). Особенностью ячейки является очень большое различие площадей поверхности электродов. Поскольку площадь поверхности индикаторного электрода (микроэлектрода) значительно меньше площади поверхности электрода сравнения, плотность тока на нем во много (несколько десятков тысяч) раз больше, чем на электроде сравнения, поэтому при включении развертки внешнего напряжения микроэлектрод поляризуется. Плотность тока на электроде сравнения значительно ниже, поэтому полагают, что он не поляризуется (потенциал его остается постоянным), но это справедливо лишь при протекании через ячейку небольших токов. Однако при регистрации вольтамперограмм может протекать довольно заметный ток, поэтому для более точных измерений рекомендуется применять трехэлектродную ячейку (см. рис. 4.27, б). Она содержит еще вспомогательный электрод (платиновая проволочка или пластинка, слой ртути на дне ячейки), служащий токоотводом от индикаторного электрода. В этом случае ток через электрод сравнения протекать не будет, и он сохраняет потенциал постоянным.
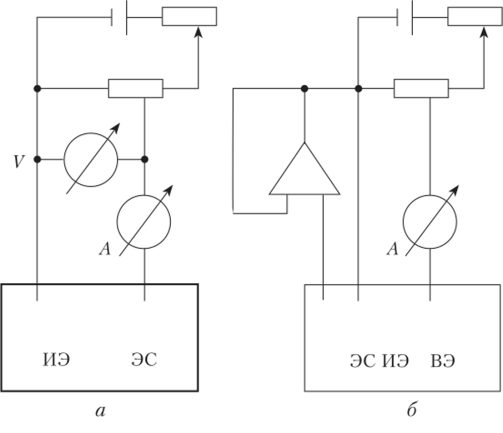
Рис. 4.27. Двухэлектродная (а) и трехэлектродная (б) ячейки для вольтамперометрических измерений:
ИЭ — индикаторный электрод; ЭС — электрод сравнения;
ВЭ — вспомогательный электрод В качестве электродов сравнения в вольтамперометрии чаще других применяют насыщенный каломельный (табулированные величины /:]/2 обычно дают относительно этого электрода), а также хлорсеребряный электрод. При определении концентрации удобно использовать слой ртути на дне ячейки (см. рис. 4.23, а), называемый обычно ртутным анодом. Недостатком этого электрода является то, что его потенциал зависит от состава раствора, контактирующего с ним.
Индикаторными электродами служат микроэлектроды из ртути, платины и токопроводящих углеродных материалов (графит, стеклоуглерод). Во время регистрации вольтамперограммы поверхность твердого (графитового или платинового) электрода не возобновляется. Поэтому, если электрод не вращается, то вольтамперограмма имеет вид, показанный на рис. 4.28 (кривая а). Спад тока после достижения максимума вызван обеднением приэлектродного слоя. Если электрод вращать, то при скорости вращения выше 400 об/мин в приэлектродном слое возникают условия для стационарной диффузии, поэтому вольтамперограмма имеет ту же форму, что и в случае капающего ртутного электрода (кривая 6). Воспроизводимость результатов на вращающемся электроде значительно выше, чем на стационарном.
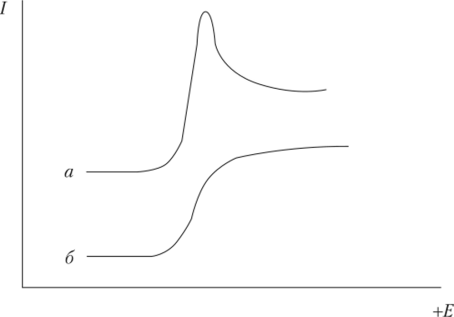
Рис. 4.28. Вольтамперограммы, полученные на стационарном (а) и вращающемся (6) твердом электроде Инверсионную вольтамперометрию применяют для определения крайне низких концентраций веществ, вплоть до 10-9 М. Существует несколько вариантов метода. Во всех вариантах первой стадией процесса является предварительное электрохимическое концентрирование определенных веществ, что приводит к существенному повышению чувствительности. Определяемое вещество концентрируют электролизом на поверхности индикаторного электрода. Электролиз проводят при потенциале предельного тока восстановления или окисления вещества при энергичном перемешивании раствора. Для полного выделения вещества из раствора понадобилось бы бесконечно большое время, что не пригодно для анализа, поэтому электролиз ведут в течение определенного и строго фиксируемого времени.
В большинстве случаев используют твердый электрод из какого-либо материала, чаще всего из спектрально чистого графита, пропитанного эпоксидной смолой с полиэтиленполиамином. Метод позволяет определять не только полярографически активные ионы, но также ионы, которые не поддаются прямому полярографированию.
Вольтамперометрический анализатор (рис. 4.29) предназначен для определения в пробах пищевых и сельскохозяйственных продуктов, экологических и биологических объектов, косметики, высокочистых материалов, руд, минералов и т. п. Zn, Cd, Pb, Си, Hg, As, Fe, Se, Sb, Sn, Bi, Mn, Co, Ni, Au, I, Ag и других веществ.
Анализатор позволяет проводить одновременный анализ трех проб, перемешивать раствор путем стабилизированной вибрации индикаторного электрода, устранять мешающее влияние кислорода и разрушать органические вещества с помощью встроенной УФ-лампы, обрабатывает анализируемый раствор инертным газом и озоном, одновременно определяет наличие Zn, Cd, Pb, Си.

Рис. 4.29. Вольтамперометрический анализатор.
Задачи
4.3.1. Каков будет предельный диффузионный ток при восстановлении иона М2+, если его концентрация 2,0−10_/l М, коэффициент диффузии 6,0−10-6 см-с-1, используют капилляр, у которого т = 2 мг/с и т = 5 с?
Решение
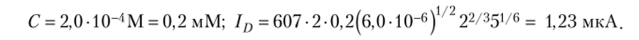
4.3.2. При полярографировании раствора были получены следующие данные.
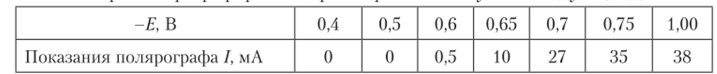
Определите высоту волны.
Решение
Высота волны определяется по точкам пересечения прямых, аппроксимирующих волну. Уравнение первой прямой.
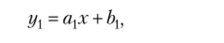
где а = b — сила тока при Е = 0. Поскольку а, = 0, у{ принимаем равным нулю. АЬ
Для второй прямой.
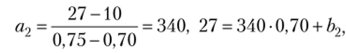
откуда Ь2 = -2.
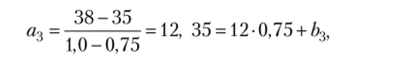
откуда Ь3 = 26.
Таким образом, решаем систему двух уравнений.
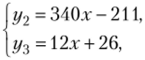
откуда х = 0,724 и у = 35. Поскольку yt = 0, то h = 35.
4.3.3. При полярографировании серии стандартных растворов Cd2+ и исследуемого раствора Cd2+ были получены следующие данные:
С, мг/мл 0,2 0,4 0,8 1,0 х
h, мм 15 30 60 75 50.
Во всех случаях брали одинаковые объемы анализируемого и стандартного растворов и добавляли одинаковое количество реагентов. Определите концентрацию раствора Cd2+.
Решение
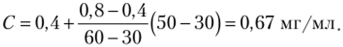
4.3.4. Определите величину предельного диффузионного тока цинка, если С = = 0,003 моль/л, D = 0,72−10-5 см2/с, т = 3 мг/с, т = 4 с.
Ответ: 25,4 мкА.
4.3.5. Для определения меди полярографическим методом была взята навеска 0,8120 г и помещена в мерную колбу вместимостью 200 мл. Затем 50 мл полученного раствора поместили в мерную колбу емкостью 100 мл и при полярографировании 20 мл этого раствора получили волну высотой 36 мм. Далее 5 мл стандартного раствора, содержащего 0,085 мг/мл меди, поместили в мерную колбу емкостью 100 мл и при полярографировании 20 мл стандартного раствора получили волну высотой 25 мм. Вычислите процентное содержание меди в испытуемом образце.
Ответ: 0,015%.
4.3.6. Для определения цинка навеску 0,9424 г руды перевели в мерную колбу вместимостью 100 мл. При полярографировании исследуемого раствора получена полярограмма 1 (см. рис. 4.30). Затем 15 мл стандартного раствора, содержащего 1 мг/мл цинка, разбавили в мерной колбе емкостью 100 мл и после полярографирования получили полярограмму 2.
Вычислите процентное содержание цинка в руде.
Решете
- 1. По нолярограмме находим высоту волны: hCT = 65 мм, hx. = 43 мм.
- 2. Определим концентрацию цинка в 100 мл стандартного раствора, т. е. в на-
hr. 39.
веске Сг= С"-г— = 15— =9,59 мг.
" ст «1
3. Рассчитаем процентное содержание цинка в навеске: в 0,9424 г руды содержит0,959 100 0,9424.
ся 0,959 г цинка, а в 100 г руды содержится х г цинка. Отсюда х =
= 1,02%.
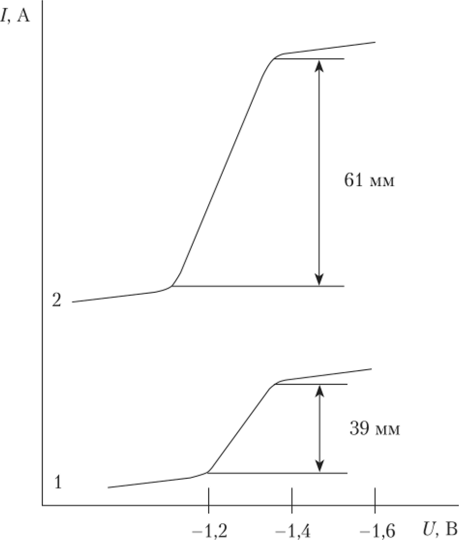
Рис. 4 JO. Подпрограмма исследуемого раствора.
4.3.7. Диффузионный ток, измеренный за время т = 5 с, равен 6,0 мкА. Какова будет его величина при т = 3 с?
Ответ: 5,51 мкА.
4.3.8. Определите концентрацию кадмия в растворе, если D = 0,72−10-5 см2/с, т = = 2,0 мг/с, т = 4,4 с, а сила тока — 10 мкА.
Ответ-. 0,0015 М.
Контрольные вопросы и задания
- 1. Что такое вольтамперометрия?
- 2. Вольтамперометрия является количественным или качественным методом анализа?
- 3. Какие свойства веществ она позволяет измерить?
- 4. Чем отличаются вольтамперометрия и полярография?
- 5. На чем основан полярографический метод?
- 6. Почему в полярографии в качестве электродов используют ртуть?
- 7. Почему в полярографии используют капельный ртутный электрод?
- 8. Как по подпрограмме определить род вещества и его количество?
- 9. Что такое остаточный ток?
- 10. Что такое предельный ток?
- 11. Как выглядят классические интегральная и дифференциальная подпрограммы?
- 12. Как выглядит полярограмма нескольких веществ?
- 13. Какие условия необходимо соблюсти при полярографическом анализе?
- 14. Зачем перед регистрацией подпрограммы нужно удалить растворенный кислород? Как это можно сделать?
- 15. Чем обусловлена высокая воспроизводимость измерений с помощью ртутного капающего электрода?
- 16. Что такое осцилляция? Полезное ли это явление?
- 17. Запишите уравнение Д. Ильковича.
- 18. Какие факторы влияют на величину предельного диффузионного тока?
- 19. Какими способами можно улучшить соотношение фарадеевского и емкостного токов?
- 20. Что такое осциллографическая полярография?
- 21. Расскажите об импульсной полярографии и ее разновидностях: нормальной и дифференциальной.
- 22. Объясните суть переменно-токовой полярографии.
- 23. Объясните принцип действия синусоидальной переменно-токовой полярографии.
- 24. Расскажите о методе квадратно-волновой переменно-токовой полярографии.
- 25. Каковы особенности ячейки для вольтамперометрических измерений по сравнению с ячейками, применяемыми в потенциометрии?
- 26. Расскажите о двухи трехэлектродной ячейках, применяемых в вольтамперометрии.
- 27. Расскажите об индикаторных микроэлектродах.
- 28. Что такое инверсионная вольтамперометрия?