Органические оксисоединения — альдегиды и кетоны

Альдегиды и кетоны образуются при окислении первичных и вторичных спиртов (с. 162). К общим методам получения альдегидов и кетонов относится гидролиз галогенпроизводных углеводородов с двумя атомами галогена у одного атома углерода. Характерными изменениями сопровождаются реакции окисления альдегидов аммиачным комплексным соединением серебра и гидроксидом меди (П). В первом случае на хорошо… Читать ещё >
Органические оксисоединения — альдегиды и кетоны (реферат, курсовая, диплом, контрольная)
Альдегиды и кетоны содержат карбонильную группу С=0. В альдегидах карбонил находится на конце углеродной цепи, и поэтому он соединен также с водородом. ГруппуСНО в целом рассматривают как функциональную группу альдегидов:
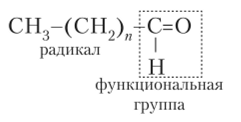
В единственном из альдегидов формальдегиде (метанале) функциональная группа связана не с углеводородным радикалом, а только с атомом водорода. В кетонах функциональная группа С=0 связана с двумя углеводородными радикалами:
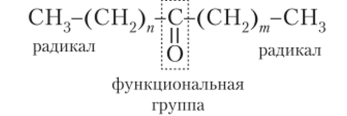
Альдегиды и кетоны с предельными радикалами имеют одну и ту же общую формулу С"Н2/гО, но первый член в гомологическом ряду альдегидов — метаналь (п = 1), а в гомологическом ряду кетонов — пропанон (п = 3). Наиболее широко известные оксисоединения — формальдегид и ацетон. Водный 37%-ный раствор формальдегида называют формалин. Он имеет характерный раздражающий запах. Формалин применяется в качестве консерванта анатомических препаратов. В разбавленном виде используется для дезинфекции кожных покровов. Ацетон служит растворителем красок, лаков, жиров, полимерных смол. Его мировое производство составляет более 3 млн т в год.
Альдегиды и кетоны — более летучие соединения, чем спирты с тем же углеродным скелетом, так как не образуют водородных связей. Метаналь при обычных условиях газ, этаиаль — вещество с температурой кипения 20 °C. Низшие альдегиды хорошо растворимы в воде. Физические и химические свойства веществ этих классов определяются наличием полярной группы С=0. Смещение электронной пары тт-связи к кислороду позволяет атому углерода принимать электронную пару реагента. Поэтому для альдегидов и кетонов особенно характерны реакции нуклеофильного присоединения (Ду), дающие очень много практически важных органических веществ разных классов. По реакционной способности оксисоединения располагаются в следующий ряд:
формальдегид «остальные альдегиды :» кетоны.
Получение альдегидов и кетонов. Формальдегид получают в больших количествах каталитическим окислением метанола, а также метана:

Не менее практически важен этаналь, чаще называемый ацетальдегид. Его получают гидратацией ацетилена (с. 152) и каталитическим окислением этилена:
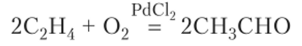
Альдегиды и кетоны образуются при окислении первичных и вторичных спиртов (с. 162). К общим методам получения альдегидов и кетонов относится гидролиз галогенпроизводных углеводородов с двумя атомами галогена у одного атома углерода.
Химические свойства альдегидов и кетонов. Оксисоединения проявляют обычное свойство органических веществ — способность гореть. Альдегиды к тому же сильные восстановители, окисляющиеся до кислот.
Характерными изменениями сопровождаются реакции окисления альдегидов аммиачным комплексным соединением серебра и гидроксидом меди (П). В первом случае на хорошо отмытой от жиров стенке сосуда оседает зеркальный слой серебра:
t 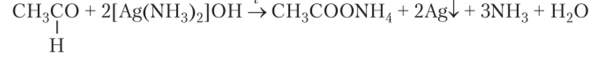
Во второй реакции выпадает оранжево-красный осадок оксида меди (1):

Реакции нуклеофильного присоединения. Альдегиды и кетоны присоединяют молекулы многих неорганических и органических веществ по механизму AN. Почти весь формальдегид в водном растворе гидратирован и находится в виде дигидроксопроизводного, подобного угольной кислоте:
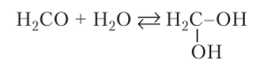
При удалении воды продукт присоединения полностью распадается и в индивидуальном состоянии не существует. Другие альдегиды гидратируются в меньшей степени, чем Н2СО, а кетоны не гидратируются.
Альдегиды присоединяют молекулы спиртов, образуя полуацетали. Нуклеофильная частица С2Н30_ присоединяется к углероду, а Н+ — к кислороду:
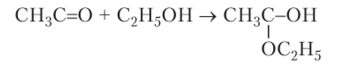
В полуацетале нет протона, который вместе с ОН-группой мог бы образовать молекулу воды. Поэтому полуацеталь, в отличие от соединения альдегида с водой, относительно устойчив. Многие другие молекулы, в которых есть подвижный протон, также присоединяются к альдегидам и кетонам.
В параграфе 163 рассмотрено образование полимерного вещества из фенола и формальдегида. Очень активный формальдегид и без участия других веществ постепенно полимеризуется в растворах. В водной среде образуется циклический продукт гриоксан.
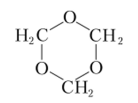
При упаривании водного раствора формальдегида в вакууме образуется белый порошок параформ (СН20)". Он применяется в горючих смесях, называемых сухой спирт. При нагревании параформ деполимеризуется, выделяя формальдегид. В присутствии извести полимеризация формальдегида приводит к образованию углеводов. Эта реакция была открыта А. М. Бутлеровым.