Рост кристаллов.
Процессы и аппараты пищевых производств

Образование новой (твердой) фазы в существующей (жидкой) возможно только при ее пересыщении, поскольку процесс требует расхода энергии на образование поверхности раздела фаз. Поэтому движущей силой процесса роста кристаллов является разность концентраций пересыщенного Спер и насыщенного растворов. Кинетику процесса роста кристаллов можно описать уравнением. Каждая грань имеет свою линейную… Читать ещё >
Рост кристаллов. Процессы и аппараты пищевых производств (реферат, курсовая, диплом, контрольная)
Образование новой (твердой) фазы в существующей (жидкой) возможно только при ее пересыщении, поскольку процесс требует расхода энергии на образование поверхности раздела фаз. Поэтому движущей силой процесса роста кристаллов является разность концентраций пересыщенного Спер и насыщенного растворов. Кинетику процесса роста кристаллов можно описать уравнением 
Однако следует заметить, что скорость роста кристаллов не равна скорости растворения, так как кристаллизация — не чисто диффузионный процесс. Этот процесс ограничен скоростью внедрения молекул в кристаллическую решетку, т. е. наряду с диффузионной стадией имеет место кристаллохимическая реакция на поверхности кристаллов. Вследствие преодоления потенциального барьера концентрация будет уменьшаться не до Снас, а до некоторого промежуточного значения на поверхности Спов. Таким образом, изменение концентрации будет происходить:
- • для диффузионной области от концентрации пересыщенного раствора в объеме Спер до Спов;
- • для кристаллохимической реакции от Спов до концентрации насыщения Снас.
Отсюда скорость процесса роста кристаллов описывается уравнениями:
• для диффузионной стадии:
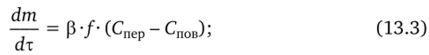
• для кристаллохимической реакции:
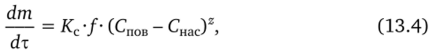
где Кс — константа скорости кристаллохимической реакции; z — показатель степени.
Приняв z=l, преобразуем уравнения (13.3) и (13.4):
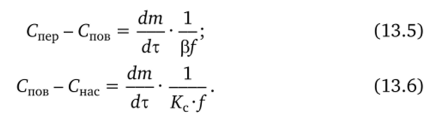
Складывая почленно правые и левые части уравнений (13.5) и (13.6), получим:
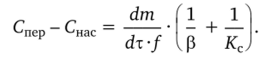
Отсюда скорость роста кристаллов:
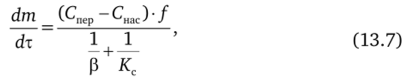
где К = * — коэффициент массопередачи.
При значительном возрастании р диффузионным сопротивлением можно пренебречь и тогда:
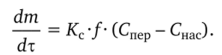
В этом случае процесс определяется кристаллохимической реакцией, что имеет место, например, при кристаллизации а-лактозы.
Разделим обе части уравнения (13.7) на р/. В результате получим уравнение линейной скорости роста:

Каждая грань имеет свою линейную скорость роста, в противном случае все кристаллы стремились бы к сферичной форме. Каждой грани характерно свое значение Кс. Двухнаправленный рост кристаллов лактозы и сахарозы был экспериментально изучен в работе (10].