Обратимая химическая реакция i-го порядка

График зависимости потока десорбирующегося из пластины газа от времени диффузионного эксперимента из дефектной среды при различных соотношениях Сю и С20 приведен на рис. 5. Интенсивное выделение происходит из образцов, в которых в начальный момент времени весь газ находился в подвижной форме. По мере увеличения начального количества газа в неподвижном виде время дегазации возрастает. При Сю=1… Читать ещё >
Обратимая химическая реакция i-го порядка (реферат, курсовая, диплом, контрольная)
Для описания нестационарной диффузии газа при наличии обратимой химической реакции 1-го порядка в пластине толщиной Н необходимо решить систему дифференциальных уравнений вида:
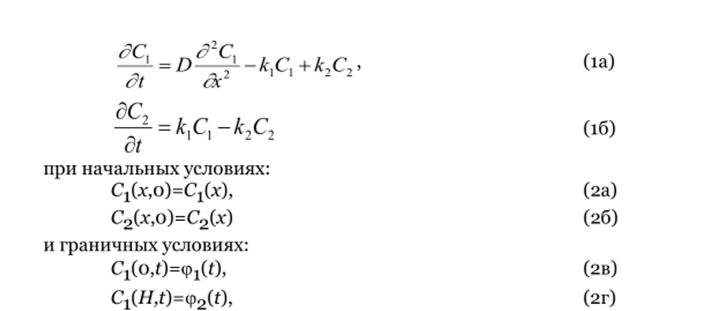
где Ci- концентрация диффузанта, С2 — концентрация неподвижного продукта реакции диффузанта с веществом пластины, Н — толщина пластины, кгик-2 — константы скоростей прямой и обратной реакции, соответственно, D — коэффициент диффузии.
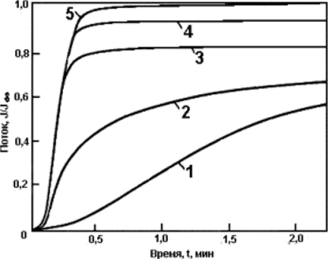
Рис. 2. Зависимость потока диффузанта на выходе мембраны от времени при различных значениях константы равновесия обратимой химической реакции:/С=ю; i -ki=ioo с*1, к-2= ю с1; 2 -ki=io сЛ к2=1 с1; з — кi=i с1, к2=0.1 с1; 4 -ki=o.i с*1, k2=o.oi с*1; 5 -ki=o.oi с к2= o. ooi с •; D/H2=i.
Здесь, при задании граничных условий рассматривалась только подвижная фаза (диффузант с концентраций Сх диффундирует в пластине с коэффициентом диффузии Di=D). Условия для неподвижной фазы (продукт реакции с концентрацией С2, его коэффициент диффузии D2=о) появляются автоматически из решения Урлб.
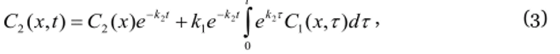
Займёмся решением системы (l) при обобщенных краевых условиях (2 и з). Подставив выражение (з) в (la), умножив его на exp(k2i) и продифференцировав результат по f, получим:
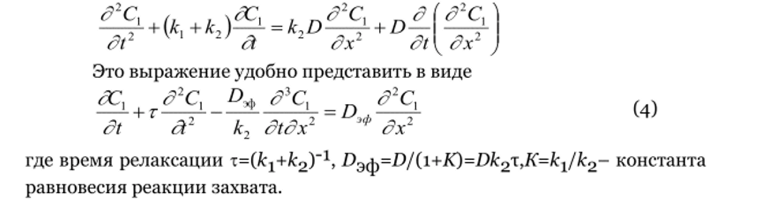
Ур.4 не эквивалентно системе (i), так как в нём нет информации о начальном распределении концентрации неподвижного вида, но оно удобно для вычисления декрементов затухания диффузионной волны (aj).
Дифференциальное уравнение для диффузии с химической реакцией будем решать методом разделения переменных Фурье. С этой целью введём в Ур.4 подстановку:




При решении задачи проницаемости плоской мембраны при взаимодействии диффузанта с материалом пластины, подчиняющемся обратимой химической реакции i-го порядка методом операционного исчисления ограничимся «классической» проницаемостью: в начальный момент вре;





Если начальный момент времени весь диффузант располагался в диффузионных путях (С2о=о), то поток диффузанта из пластины.
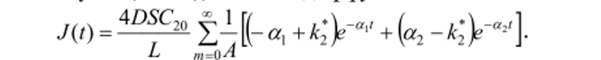
График зависимости потока десорбирующегося из пластины газа от времени диффузионного эксперимента из дефектной среды при различных соотношениях Сю и С20 приведен на рис. 5. Интенсивное выделение происходит из образцов, в которых в начальный момент времени весь газ находился в подвижной форме. По мере увеличения начального количества газа в неподвижном виде время дегазации возрастает. При Сю=1 (т.е. если до начала эксперимента газ находился в неподвижном виде) потокДО достигает максимального значения и лишь затем начинает снижаться.
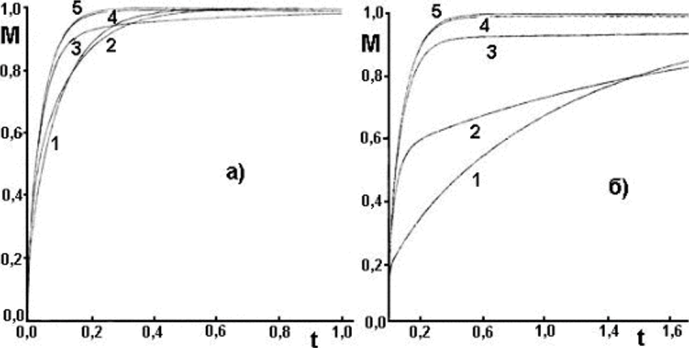
Рис. 4. Количество диффузанта, сорбированное пластиной к моменту времени t при.
i обратной реакции, D/H2=1. a) K= 1, 1 —, 1,4 — ki=o, i, k2=o, oi, 5 — ki=o, oi, k2= k2=1,3 — ki=iy k2=0,1,4 — A: i=o, i; k2=0,01,5
различных значениях констант прямой i ki=ioo, к2=ю, 2 — ki=w, k2=i, 3 — ki=i, k2=c 0,001. 6) K= 10,1 — ki=ioo, k2=10, 2 — ki=io, — ki=o, oi; k2 =0,001.
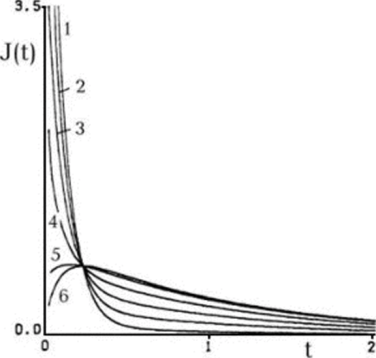
Все кинетические кривые дегазации пересекаются в точкемаксимума кривой для C20=i. После достижения времени fMaKc=(lna2-lnai)/2 график идёт тем выше, чем больше газа первоначально находилось в неподвижном виде.
Рис. 5. Зависимость от времени потока диффузанта из пластины при постоянной температуре, D/L2=1, К= 1, k 1—к‘2=1, 1 — Сю=1, С2о= 0,001, 2 — 0,75; 0,25; з — 0,5; 0,5; 4 — 0,25:0,74; 5 — 0,2; 0,8; 6 — Сю=о, С20 = 1.