Свойства и превращения глицерофосфолипидов

Некоторая часть фосфолипидов не выделяется из масел или выделяется только с помощью специальных приемов гидратации масел (негидратируемые фосфолипиды). По современным представлениям — это комплексные соединения фосфолипидов с ионами металлов (Са2+, Mg2+, Cu2+, Fe2+ и Fe3+; последние являются катализаторами процессов окисления), а также соединения со стеролами и алифатическими спиртами… Читать ещё >
Свойства и превращения глицерофосфолипидов (реферат, курсовая, диплом, контрольная)
Глицерофосфолипиды — бесцветные вещества, без запаха, хорошо растворимы в жидких углеводородах и их галогенпроизводных, отдельные группы различаются растворимостью в спиртах, ацетоне. Они существуют в нескольких полимерных формах и плавятся в две стадии. Обладают оптической активностью. Выделенные из природных объектов фосфолипиды — аморфные вещества, перекристаллизованные из органических растворителей — имеют кристаллическую структуру.
Химические превращения глицерофосфолипидов обусловлены характером и строением структурных компонентов и видами химических связей. Для них характерны реакции гидролиза кислотами и щелочами.
Взаимодействие глицерофосфолипиды-углеводы:
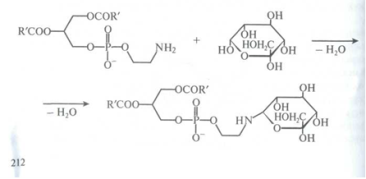
Некоторая часть фосфолипидов не выделяется из масел или выделяется только с помощью специальных приемов гидратации масел (негидратируемые фосфолипиды). По современным представлениям — это комплексные соединения фосфолипидов с ионами металлов (Са2+, Mg2+, Cu2+, Fe2+ и Fe3+; последние являются катализаторами процессов окисления), а также соединения со стеролами и алифатическими спиртами.
В результате энзимической и химической модификации в промышленности получают различные виды производных фосфолипидов (лецитинов): гидролизованные лецитины, гидроксилированные, ацилированные с различными гидрофильно-липофильными характеристиками. Они нашли широкое применение в пищевой промышленности.