Результаты исследования и их обсуждение

Таким образом, применение УТ для коррекции андрогенной недостаточности у мужчин, страдающих пароксизмальной формой ФП, оказывало благоприятное влияние не только на андрогенный статус пациентов, но и на частоту и продолжительность приступов аритмии, психовегетативные расстройства, качество жизни больных. Полученные результаты свидетельствуют о полезности дальнейшего изучения гендерных подходов… Читать ещё >
Результаты исследования и их обсуждение (реферат, курсовая, диплом, контрольная)
Клинические проявления недостаточности андрогенов были выявлены с помощью опросника AMS у больных стенокардией в 85,5% случаев, у пациентов с гипертонической болезнью — в 86,4% случаев, у мужчин, страдающих фибрилляцией предсердий — в 81,4% случаев. Средний балл по шкале опросника AMS достаточно тесно коррелировал с уровнем тестостерона (r = - 0,49, р<0,001). Концентрация общего тестостерона в обследованной группе мужчин с кардиоваскулярной патологией (10,7±4,2 нмоль/л) оказалась ниже того уровня (12 нмоль/л), с которого начинают проявляться клинические симптомы андрогенной недостаточности. Дефицит тестостерона определялся у 299 (53%) больных, что превышает распространенность данного состояния в популяции в 2 раза (Pugh P.J. 2003). Андрогенодефицитное состояние, установленное по показателю ИСА, выявлялось еще чаще — у 69,3% обследованных мужчин. Cамый низкий уровень тестостерона определялся у больных ИБС, стабильной стенокардией напряжения — 9,8±4,3 нмоль/л. У пациентов с гипертонической болезнью и фибрилляцией предсердий концентрация тестостерона составила 10,3±3,7 и 12,0±4,9 нмоль/л соответственно.
При корреляционном анализе между возрастом обследованных больных и концентрацией тестостерона была выявлена слабая связь (r = 0,14, p>0,05). При этом содержание глобулина, связывающего половые стероиды (ГСПС), с возрастом увеличивалось (r=0,47; р=0,009). Следовательно, у мужчин с ССЗ с возрастом происходит снижение индекса свободных андрогенов. В результате даже при нормальном уровне тестостерона у больного может существовать андрогенодефицитное состояние.
Установлено, что больные с андрогенодефицитом чаще вели малоподвижный образ жизни, имели бульшую стрессовую нагрузку в течение предшествовавшего года и более высокие показатели уровня тревоги и депрессии, чем мужчины с нормальным уровнем тестостерона. По-видимому, хронический психосоциальный стресс, для которого характерно развитие тревожно-депрессивных расстройств, в сочетании с низкой физической активностью создает условия для преждевременного снижения выработки андрогенов.
Было установлено наличие обратной корреляции между концентрацией тестостерона и индексом массы тела (r = - 0,42; p<0,001). Кроме того, обнаружено наличие связи андрогенодефицита с абдоминальным ожирением, определявшимся при окружности талии более 102 см (r = - 0,49; p <0,001). В данном исследовании была предпринята попытка установить связь гипотестостеронемии с увеличением содержания жировой ткани (СЖТ) в организме, а также с её накоплением в области живота. Измерение СЖТ производилось биоимпедансным методом, с помощью которого можно получить достаточно точные данные о жировой массе тела (Boyanov V.A. и соавт., 2003). Было установлено наличие обратной корреляционной связи уровня тестостерона с СЖТ (r = - 0,52; р<0,001). Следовательно, избыточная масса тела у больных ССЗ и андрогенным дефицитом действительно ассоциируется с увеличением массы жировой ткани (ЖТ). Было обнаружено, что наибольший коэффициент корреляции с уровнем тестостерона (r = - 0,6; р<0,001) имеет отношение массы ЖТ (МЖТ) к окружности талии (ОТ).
Уровень тестостерона в крови обратно коррелировал с ЧСС при госпитализации, концентрацией в крови холестерина, ХС ЛПНП, протромбиновым индексом и ИММЛЖ. Было установлено наличие прямой корреляционной связи уровня тестостерона с качеством жизни (КЖ) мужчин (r = 0,33; р=0,004). Снижению КЖ мужчин способствовали повышенные уровни тревожности, депрессии, вегетативной дистонии, нарушения физического функционировании и сексуальные расстройства при гипотестостеронемии.
Особенности клинической картины стенокардии в зависимости от наличия или отсутствия дефицита андрогенов Для изучения влияния андрогенного дефицита и его коррекции на течение стенокардии напряжения было обследовано 214 мужчин, средний возраст которых составил 51,1±6,2 года. У 65,9% больных было установлено наличие андрогенодефицитного состояния. При андрогенодефицитном состоянии ангинозный синдром часто имел атипичный характер, когда боль в грудной клетке носила колюще-давящий характер и сопровождалась чувством жара в груди (с распространением на лицо) и потливостью.
Приступы стенокардии у таких больных возникают на фоне выраженных вегетативных расстройств с сердцебиением, чувством жара, нехватки воздуха, гипергидрозом. Атипичный характер ангинозной боли в случаях с андрогенным дефицитом встречался в 35,1% случаев, а при его отсутствии — в 19,2% (р = 0,01).
В группе мужчин с андрогенным дефицитом существенно выше была доля больных с частыми (3−5 раз в сутки) приступами стенокардии по сравнению с пациентами без дефицита тестостерона (45,4% и 30,1% соответственно). Обратила на себя внимание в 2 раза бульшая частота выявления низкой толерантности к физической нагрузке (приступы стенокардии при ходьбе на расстояние менее 100 м) у больных с андрогенным дефицитом.
Был проведен анализ результатов нагрузочного теста у мужчин с различным уровнем тестостерона (табл. 2). Больные с андрогенодефицитом были способны выполнять менее продолжительную работу и в меньшем объеме по сравнению с пациентами того же возраста без дефицита тестостерона. У них также отмечалась более низкая средняя ЧСС, при которой развивался приступ стенокардии либо появлялась депрессия сегмента ST ишемического типа. Кроме того, у больных стенокардией с дефицитом андрогенов значительно чаще развивалась избыточная гипертензивная реакция на нагрузку.
Таблица 2.
Результаты ВЭМ-пробы у больных с различным уровнем тестостерона.
Показатели ВЭМ. | На высоте нагрузки. | |||||
ДН, сек. | ПМ, Вт. | ОВР, Вт. | ЧСС,. (депрессия ST. на 1 мм). | САД, мм. рт.ст. | ДП,. усл. ед. | |
Группа с андрогенодефицитом (n=141). | ||||||
302±26. | 98±10. | 401±51. | 112±11. | 178±11. | 199±18. | |
Группа без андрогенодефицита (n=73). | ||||||
353±31*. | 120±13*. | 466±62*. | 118±12*. | 166±10*. | 196±16. | |
Примечания: ДН — длительность нагрузки, ПМ — пороговая мощность,.
ОВР — объем выполненной работы, ДП — двойное произведение;
* - значимость различий p<0,001.
Под данным СМ ЭКГ, у больных с андрогенным дефицитом в сравнении с пациентами с нормальным уровнем тестостерона отмечалось большее количество эпизодов ишемической депрессии сегмента ST (5,3±1,5 против 4,7±1,3, р=0,01). Эпизоды безболевой депрессии сегмента ST наблюдались у 38% мужчин с андрогенным дефицитом, а у пациентов с нормальным уровнем тестостерона — только в 24% случаев (р < 0,001).
У больных стенокардией с дефицитом тестстерона отмечались более высокие показатели общего ХС, ХС ЛПНП и более низкие — ХС ЛПВП. Наличие гиперхолестеринемии (более 5,0 ммоль/л) установлено у 90,4% мужчин с дефицитом тестостерона и у 69,9% - без андрогенного дефицита (р<0,001). Кроме того, у мужчин с дефицитом тестостерона выше были среднее значение протромбинового индекса (93,4±7,5 и 91,1±3,7%, р=0,008) и глюкозы крови (6,05±0,95 против 5,22±0,29 ммоль/л, р< 0,001), чем в группе без андрогенного дефицита.
У больных стенокардией с андрогенной недостаточностью показатель качества жизни (КЖ) был существенно ниже, чем у пациентов без дефицита тестостерона: — 7,9±3,61 и — 5,6±3,72 балла соответственно (p<0,001). У больных с андрогенодефицитом чаще выявлялись нарушения физического функционирования, ограничения, связанные с необходимостью лечиться, изменения в половой сфере. Также больные из этой группы достоверно чаще испытывали затруднения во взаимоотношениях с близкими, переживали необходимость ограничений в питании, курении и в проведении досуга.
Влияние заместительной гормональной терапии на клиническую картину стенокардии и андрогенный статус мужчин Показатели, характеризующие андрогенный статус больных на 90-й и 180-й день наблюдения и лечения, представлены в табл. 3. Было установлено снижение при ЗГТ уровня ГСПС, который через 6 месяцев терапии был ниже исходного на 21,5%, что привело, при одновременном увеличении концентрации общего тестостерона, к росту ИСА на 54,7%. Через 6 месяцев приема УТ 92% пациентов отметили повышение либидо, частоты ночных эрекций, повышение способности к проведению половых актов и их частоты, возрастание удовлетворенности половой жизнью. У мужчин группы сравнения, не получавших УТ, выраженность клинических признаков гипогонадизма осталась прежней.
В основной группе на 180-й день произошло снижение частоты ангинозных приступов в сравнении с исходными данными на 50,7% (p<0,05). В группе сравнения частота приступов также уменьшилась, однако в меньшей степени — на 22,5% через 6 мес, что статистически значимо отличалось от результатов лечения больных основной группы (p<0,05).
Таблица 3.
Динамика показателей, характеризующих андрогенный статус, у больных стенокардией.
Показатель. | Основная группа. | Группа сравнения. | |||
Исходно. | 6 мес. | Исходно. | 6 мес. | ||
AMS, баллы. | 42,4±7,8. | 27,3±6,8. | 43,1±8,2. | 44,5±8,3. | |
Тестостерон, нмоль/л. | 7,8±3,0. | 13,2±2,9. | 7,6±3,1. | 7,5±3,0. | |
ГСПС, нмоль/л. | 32,1±6,7. | 25,2±5,3. | 32,7±6,3. | 32,9±6,1. | |
ИСА, %. | 31,6±8,2. | 48,9±7,9. | 32,2±8,8. | 32,1±8,6. | |
Тестостерон свободный, пмоль/л. | 172±45. | 248±54. | 170±51. | 173±49. | |
Тестостерон биодоступный, нмоль/л. | 3,1±1,4. | 4,1±1,3. | 3,2±1,5. | 3,2±1,2. | |
Примечание: показатели пациентов основной группы на 180-й день статистически значимо отличались от исходных данных и результатов 3-х месяцев (p<0,05) по ранговому критерию Friedman для нескольких независимых переменных, а также от показателей группы сравнения в соответствующие периоды согласно тесту Kruskal-Wallis (p<0,05).
Количество потребляемых в неделю таблеток нитроглицерина в основной группе уменьшилось 56,9%, в группе сравнения — на 30,8% (p<0,05) Клинический эффект применения препарата тестостерона выразился также в изменении функционального класса (ФК) стенокардии.
Отмечено, что у 34,3% пациентов основной группы произошло уменьшение ФК на 1 ступень, у 4,3% - на 2 ступени. При этом в группе сравнения ФК уменьшился на 1ступень лишь у 15,2% пациентов, на две — ни в одном случае, а у 4,5% - увеличился на 1 ступень.
На 180-й день всем пациентам было проведено СМ ЭКГ. Изменения частоты и продолжительности ишемических эпизодов отражены в табл. 4. На фоне приема УТ через 6 месяцев отмечено статистически значимое снижение количества и продолжительности эпизодов депрессии сегмента ST (как болевых, так и безболевых).
В группе сравнения также наблюдалось снижение выраженности исходных ишемических изменений, однако, в меньшей степени по сравнению с основной группой (p<0,05).
Таблица 4.
Результаты суточного мониторирования ЭКГ у больных стенокардией.
Показатель. | Основная группа (n=69). | Группа сравнения (n=65). | |||
Исх. | 6 мес. | Исх. | 6 мес. | ||
Среднее кол-во эпизодов болевой и безболевой ишемии со снижением сегмента ST. | 5,1±1,5. | 2,2±0,4*. | 5,2±1,4. | 4,3±1,2#. | |
Средняя продолжительность эпизодов болевой и безболевой ишемии со снижением сегмента ST, мин. | 87±6. | 36±5*. | 89±7. | 75±8#. | |
Среднее кол-во эпизодов безболевой ишемии с длительным (более 10 мин) снижением сегмента ST. | 1,8±0,41. | 1,0±0,3. | 1,9±0,39. | 1,6±0,2#. | |
Среднее количество эпизодов болевой ишемии с длительным (более 10 мин) снижением сегмента ST. | 3,3±0,22. | 1,3±0,14*. | 3,2±0,21. | 2,9±0,23#. | |
* - р<0,05 по сравнению с исходными показателями основной группы; # - р<0,05 по сравнению с показателями основной группы через 6 мес.
По данным ВЭМ-пробы, на фоне лечения УТ наблюдалось статистически значимое повышение толерантности к физической нагрузке, как по мощности, так и по объему выполненной работы (табл. 5).
В основной группе отмечен статистически значимый прирост через 6 мес лечения (по сравнению с исходными) таких показателей, как длительность нагрузки, пороговая мощность, объем выполненной работы, «двойное произведение».
Таблица 5.
Результаты ВЭМ-пробы в сравниваемых группах.
Период обследования. | Показатели ВЭМ. | На высоте нагрузки. | |||||
ДН. (сек). | ПМ. (Вт). | ОВР. (Вт· мин). | ЧСС,. (депрессия ST на 1 мм). | АДс. (мм рт.ст.). | ДП. (усл. ед). | ||
Основная группа (андриол). | |||||||
До лечения. | 302±26. | 90±7. | 401±51. | 118±11. | 166±10. | 195±11. | |
6 мес. | 389±25*. | 135±10*. | 857±49*. | 129±12*. | 152±10*. | 210±12*. | |
Группа сравнения. | |||||||
До лечения. | 289±25. | 92±8. | 409±52. | 120±12. | 158±11. | 189±13. | |
6 мес. | 290±23#. | 98±6#. | 438±51#. | 122±11#. | 159±12. | 191±14#. | |
Примечания: ДН — длительность нагрузки, ПМ — пороговая мощность,.
ОВР — объем выполненной работы, ДП — двойное произведение;
*- p<0,05 по сравнению с исходными данными в основной группе;
# - p<0,05 по сравнению с показателями 6 мес основной группы Пороговая ЧСС, при которой развивалась депрессия ST на 1 мм, возросла через 6 мес до 129±12 уд/мин (p<0,05). Хотя у больных, принимавших УТ, проба прекращалась из-за появления ангинозного болевого синдрома, последний, как правило, развивался на фоне бульшего, по сравнению с исходным, объема выполненной работы.
В табл. 6 отражены изменения липидного спектра, уровня глюкозы и протромбинового индекса в сравниваемых группах. Было установлено, что уровень общего холестерина (ХС) и ХС ЛПНП за 6 месяцев наблюдения и лечения снизился как в основной группе, так и в группе сравнения, поскольку больным при включении в исследование был назначен прием статинов.
Однако степень этого снижения была различной. Так, у пациентов, получавших УТ, через 6 месяцев уровень ХС уменьшился на 24,1%, ХС ЛПНП — на 33,3%, в то время как в группе сравнения это снижение составило 14,7% и 17,1% соответственно.
Сывороточная концентрация ХС ЛПВП в основной группе повысилась за время лечения с 0,92±0,12 до 1,2±0,11 ммоль/л, а в группе сравнения существенно меньше — с 0,9±0,12 до 0,97±0,1 ммоль/л (значимость различий с основной группой р=0,01).
Таблица 6.
Динамика биохимических показателей у больных стенокардией за 6-ти месячный период.
Показатель. | Основная группа. | Группа сравнения. | |||
Исходно. | 6 мес. | Исходно. | 6 мес. | ||
Холестерин, ммоль/л. | 6,2±1,4. | 4,7±1,2#. | 6,1±1,3. | 5,2±1,3*. | |
ХС ЛПНП, ммоль/л. | 4,2±1,2. | 2,8±1,2#. | 4,1±1,3. | 3,4±1,2*. | |
ХС ЛПВП, моль/л. | 0,92±0,12. | 1,2±0,11#. | 0,9±0,11. | 0,97±0,1*. | |
Гемоглобин, г/л. | 136±7,8. | 140±7,7. | 137±7,6. | 135±7,5. | |
Протромбиновый индекс, %. | 94,1±8,2. | 91,1±8,0. | 93,7±8,0. | 93,9±8,2*. | |
Глюкоза, ммоль/л. | 6,0±0,9. | 5,2±0,7#. | 5,9±0,8. | 5,6±0,5. | |
* - отличия от показателей основной группы на 180-й день статистически значимы (p<0,05); # - p<0,05 для отличия от исходных данных основной группы.
При анализе эффективности липид-снижающей терапии необходимо принять во внимание уровень комплаентности пациентов. Если в начале терапии статины были предписаны для амбулаторного приема всем больным, то опрос участников исследования на 180-й день показал, что в основной группе (ЗГТ) через 6 месяцев продолжали принимать аторвастатин 32% мужчин, в группе сравнения (без ЗГТ) — 35% пациентов.
Это не могло не сказаться на относительно небольшом снижении уровней ХС и ХС ЛПНП у пациентов группы сравнения. По данным К. Г. Гуревич и Ю. Б. Белоусова (2004), Perreault S. с соавт. (2009) приверженность приему статинов в реальной клинической практике невелика. В то же время приверженность приему ундеканоата тестостерона в основной группе была близка к 100%. Следовательно, достигнутое на фоне приема андриола снижение уровней ХС и ХС ЛПНП, а также повышение ХС ЛПВП нельзя объяснить только действием статинов.
Был проведен анализ влияния ЗГТ на ряд показателей, характеризующих статус ожирения (табл. 7). Установлено, что на протяжении 6-ти месячного периода у пациентов основной группы происходило постепенное снижение избыточной массы тела, причем именно за счет уменьшения содержания жировой ткани в организме (преимущественно в области живота).
При лечении больных стенокардией и андрогенодефицитом с применением УТ отмечено снижение уровня депрессии с 10,8±3,7 до 5,9±3,1 баллов (р<0,001). В клиническом плане это означало уменьшение выраженности таких симптомов, как тоска, апатия, чувство бесперспективности лечения, а также улучшение сна. Снижение суммарного балла по шкале тревожности проявлялось в уменьшении внутреннего напряжения, чувства беспокойства (в том числе за состояние своего здоровья).
Таблица 7.
Динамика показателей, характеризующих избыточную массу тела.
Показатель. | Основная группа. | Группа сравнения. | |||
Исх. | 6 мес. | Исх. | 6 мес. | ||
ИМТ, кг/м2 | 31,2±7,5. | 27,5±7,2. | 31,1±7,7. | 32,5±7,4*. | |
ОТ, см. | 111±16. | 103±13. | 110±17. | 112±15*. | |
ОТ/ОБ. | 1,0±0,06. | 0,92±0,04. | 1,0±0,05. | 1,1±0,05*. | |
СЖТ, %. | 30,4±5,5. | 26,4+5,2. | 30,6±5,2. | 31,2±5,5*. | |
МЖТ/ОТ, г/см. | 274±39. | 231±30. | 271±37. | 278±30#. | |
* - p<0,05; # - p<0,01 по сравнению с показателями основной группы на 180-й день; СЖТ — содержание жировой ткани (в организме); МЖТ — масса жировой ткани.
Менее выраженными стали в основной группе также и проявления синдрома вегетативной дистонии (СВД). У 78,7% мужчин значительно уменьшилась потливость, у 62,2% больных наблюдалось уменьшение неприятных ощущений в области сердца, у 47,5% пациентов — ощущения сердцебиения, «замирания» сердца, у 43,4% - чувства похолодания и онемения конечностей, у 40,3% - приступообразных головных болей. В группе сравнения повторное тестирование на 180-й день не показало статистически значимых изменений уровней тревоги, депрессии и вегетативной дистонии.
Мужчины, принимавшие УТ, отмечали постепенное уменьшение ограничений в образе жизни, вызванных основным заболеванием, в результате чего уровень их КЖ повысился с — 8,0±3,7 балла (исходно) до — 5,7±2,5 балла на 180-й день (p<0,01). В то же время в группе сравнения динамики КЖ отмечено не было. При анализе отдельных причин снижения КЖ было установлено, что у мужчин, получавших ЗГТ, реже выявлялись нарушения физического функционирования, ограничения во взаимоотношениях с близкими и негативные изменения в половой сфере, чем у пациентов, у которых не проводилась коррекция андрогенного дефицита.
За период наблюдения неблагоприятные коронарные события в основной группе отмечены в 2,8% случаев, в то время как в группе сравнения — в 18,6% случаев (значимость различия р=0,002). В отношении частоты летального исхода между группами статистически значимых различий установлено не было. Однако у пациентов, получавших УТ, отмечена меньшая частота госпитализации по поводу нестабильной стенокардии (5,6% vs. 17,1%; р=0,03), а также тенденция к меньшей частоте развития ИМ (р=0,058). Для больных, получавших УТ, было рассчитано снижение относительного риска (СОР) неблагоприятных событий, которое составило 0,54 по отношению к группе сравнения (р=0,0022).
Механизмы клинического эффекта ЗГТ у больных ИБС, по-видимому, не ограничиваются влиянием только на липидный спектр крови. Имеются данные о том, что гипотестостеронемия способствует воспалительному процессу в атеросклеротической бляшке, тем самым, ускоряя её рост и повышая ранимость (Gornstein R.A. и соавт., 1999; Khosla S. и соавт., 2002). В работе Е. Н Арининой (2007) было показано, что при заместительной андрогенной терапии снижаются уровни провоспалительных цитокинов — С-РБ, ТНФ-б, ИЛ-6. Следовательно, длительная ЗГТ у больных стенокардией и андрогенным дефицитом может оказывать благоприятное влияние на течение и исходы ИБС посредством торможения воспаления и повышения устойчивости атеросклеротической бляшки к повреждению.
Особенности клинической картины гипертонической болезни в зависимости от наличия или отсутствия дефицита андрогенов Под наблюдением находилось 162 мужчины с гипертонической болезнью, средний возраст которых был 48,9±9,2 года. Давность заболевания в среднем составила 7,1±4,2 года. Гипертоническая болезнь (ГБ) I стадии была у 35 больных (21,6%), II стадии — у 127 (78,4%). Артериальная гипертензия 1-й степени отмечалась у 19 (11,7%) больных, 2-й степени — у 82 (50,6%), 3-й степени — у 61 (37,7%) пациентов.
Клинические симптомы гипогонадизма определялись у 60% мужчин. Андрогенодефицитное состояния по уровню общего тестостерона выявлено у 51,9% больных, а по показателю ИСА — у 58,7% мужчин. Снижение тестостерона ассоциировалось с курением (r=0,32; p=0,021), гиподинамией (r=0,34; p=0,02), абдоминальным ожирением (r=-0,63; p=0,008), повышенными уровнями стрессовой нагрузки (r=-0,4; p=0,012), тревоги (r=-0,32; p=0,021), депрессии (r=-0,34; p=0,02), вегетативной дистонии (r=-0,36; p=0,022).
Выявлена сильная обратная корреляция уровня тестостерона с показателями гипертрофии миокарда левого желудочка — толщиной задней стенки (r=-0,72; p<0,001) и межжелудочковой перегородки (r=-0,77; p<0,001), а также ИММЛЖ (r=-0,8; p<0,008). КЖ больных при снижении тестостерона ухудшалось. Средний уровень АД у больных с дефицитом тестостерона (САД 170,2±19,1 мм рт.ст., ДАД 102,9±13,8 мм рт.ст.) был статистически значимо более высоким, чем в группе с нормальным уровнем андрогенов (САД 161,3±18,7, ДАД 98,4±12,6 мм рт.ст.; p<0,05).
В целом, для мужчин, страдающих ГБ и приобретенным андрогенодефицитом, свойственна бульшая выраженность стрессовой нагрузки, тревоги, депрессии, вегетативной дистонии, абдоминального ожирения и гипертрофии миокарда левого желудочка, что находит свое отражение в снижении качества их жизни по сравнению с больными, имеющими нормальный уровень тестостерона.
Результаты коррекции андрогенного дефицита у больных гипертонической болезнью Для суждения о влиянии заместительной гормональной терапии на течение ГБ 84 пациента с андрогенным дефицитом были случайным образом разделены на 2 группы по 42 человека в каждой: основную (антигипертензивная терапия + УТ) и группу сравнения (только антигипертензивное лечение).
ЗГТ способствовала повышению уровней общего тестостерона с 9,0 (7,1−11,2) до 13,1 (11,6−15,2) нмоль/л и свободного — с 3,3 (2,9−3,6) до 3,9 (3,5−4,1) нмоль/л. Клинические проявления андрогенного дефицита, определяемые с помощью анкеты AMS, значительно уменьшились за время лечения: с 38,2 (32−49) баллов исходно 26 (24−29) баллов через 6 мес. В группе сравнения статистически значимых изменений концентрации андрогенов в крови и суммарного балла шкалы AMS выявлено не было (p>0,05). У мужчин, принимавших андриол, значительно улучшились сексуальные функции. Так, если до начала лечения 80% мужчин отмечали снижение либидо, частоты эрекций, увеличение длительности полового акта без удовлетворения, то через 6 месяцев терапии — лишь 45% (p<0,001).
Уровни САД и ДАД в каждой из наблюдаемых групп значимо снизились по сравнению с исходными показателями.
Однако, у мужчин, получавших УТ, уровень САД через 6 месяцев оказался более низким, чем у пациентов из группы сравнения (p<0,01). Изменения АД по сравнению с исходным уровнем представлены в табл. 8. В основной группе целевой уровень АД (согласно Российским национальным рекомендациям экспертов ВНОК 2004 г.) был достигнут в 82,9% случаев, в группе сравнения — в 67,3% случаев (p<0,001).
Механизмы влияния тестостерона на регуляцию уровня АД в организме изучены пока явно недостаточно. Однако, как показали экспериментальные исследования (Channer K.S., Jones T.H., 2003), с определенностью можно сказать, что тестостерону присуще прямое вазодилатирующее действие, которое связано с блокадой медленных кальциевых каналов гладкомышечных клеток сосудов.
Таблица 8.
Динамика АД в сравниваемых группах за 6-ти месячный период.
Показатель. | Основная групп па. | Группа сравнения. | |||
Исходно. | 6 мес. | Исходно. | 6 мес. | ||
САД, мм рт. ст. | 171 (159−184). | 132 (124−141)*. | 169 (157−186). | 141(135−149) # | |
ДАД, мм рт. ст. | 102 (95−106). | 84 (80−89). | 103 (96−108). | 85(81−92). | |
* - различия с исходными данными значимы (p<0,001) по критерию Wilcoxon; # - различия с результатами 6-ти мес основной группы значимы (p<0,01) по критерию Mann-Whitney.
Для оценки влияния терапии тестостероном на состояние выраженности гипертрофии левого желудочка через 6 месяцев всем пациентам было проведена ЭхоКГ.
Установлено, что у пациентов обеих групп на 180-й день произошло уменьшение КДР ЛЖ и снижение ИММЛЖ, поскольку все они получали антигипертензивную терапию. Однако, в основной группе отмечено более значительное снижение такого важного показателя гипертрофии миокарда, как ИММЛЖ, которое составило 13,7% против 9,9% в группе сравнения (p<0,001).
Результаты клинико-психологического тестирования показали, что в основной группе произошло статистически значимое снижение уровней тревоги и депрессии по сравнению с исходными показателями (табл. 9). Кроме того, было получено достоверное уменьшение выраженности синдрома вегетативной дистонии (СВД) в группе пациентов, получавших УТ. В группе сравнения не отмечено значимой динамики исходных уровней тревоги, депрессии и вегетативной дистонии.
Наряду со снижением уровня АД у мужчин, получавших УТ, отмечено снижение ИМТ и содержания жировой ткани в организме (СЖТ), уменьшение ОТ и показателя МЖТ/ОТ (рис. 1).
Таблица 9.
Результаты клинико-психологического тестирования больных ГБ на 180-й день.
Показатель. | Основная группа. | Группа сравнения. | |||
Исходно. | 6 мес. | Исходно. | 6 мес. | ||
Тревога, балл. |
|
|
|
| |
Депрессия, балл. |
|
|
|
| |
СВД, балл. |
|
|
|
| |
* - различия с исходными данными значимы (p<0,01) по критерию Wilcoxon; # - различия с результатами 6-ти мес основной группы значимы (p<0,01) по критерию Mann-Whitney.
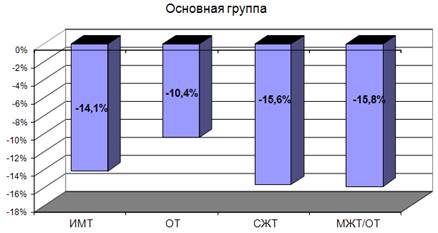
Рис. 1. Динамика показателей, характеризующих избыточную массу тела, у пациентов c ГБ основной группы. Прим.: СЖТ — содержание жировой ткани (в организме); МЖТ — масса жировой ткани.
Были проанализированы изменения отдельных ограничений, влияющих на общий уровень КЖ. Наиболее выраженные различия между группами были установлены по субшкале «негативные изменения половой сферы».
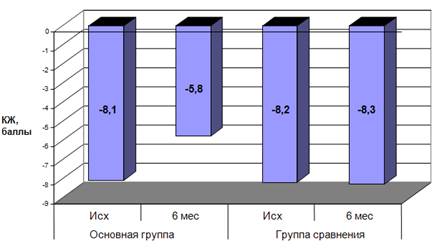
Рис. 2. Изменения КЖ у больных ГБ сравниваемых групп на 180-й день.
До включения в исследование доли мужчин, имевших сексуальные проблемы, были сопоставимы (73,8% в основной группе и 76,2% в группе сравнения). При опросе на 180-й день оказалось, что доля мужчин, имевших затруднения в половой сфере, на фоне приема андриола снизилась до 47,6% (p0,05).
По истечении 6-ти месячного периода лечения было проведено исследование КЖ пациентов сравниваемых групп. Как показано на рис. 2, у пациентов, получавших УТ, произошло статистически значимое повышение исходного уровня КЖ (р0,05).
Появившиеся в последнее время сообщения (Yeap B.B. и соавт., 2009) о том, что низкий уровень тестостерона является предиктором развития инсультов и транзиторных ишемических атак, делают актуальными дальнейшие исследования, призванные установить, может ли андрогенная заместительная терапия предупреждать развитие цереброваскулярных заболеваний у мужчин, страдающих ГБ.
Особенности клинической картины фибрилляции предсердий в зависимости от наличия или отсутствия дефицита андрогенов Было обследовано 188 мужчин, средний возраст которых составил 52,5±6,5 лет. Все больные страдали пароксизмами ФП с частотой возникновения (по анамнестическим данным) от ежедневных до 3−4 раз в год, продолжительностью от нескольких минут до 48 часов. Давность заболевания составила от 1,5 до 11 лет (в среднем — 5,3±3,8 лет). У большинства обследованных (81,4%) выявлены клинические симптомы недостаточности андрогенов различной степени. Уровень тестостерона ниже 12 нмоль/л выявлен у 93 (49,5%) мужчин. По уровню ИСА доля мужчин с андрогенной недостаточностью была еще больше — 55,9%.
Корреляционный анализ позволил установить, что сниженный уровень тестостерона ассоциировался с избыточной массой тела, абдоминальным ожирением, курением, повышенными уровнями тревоги, депрессии, вегетативной дистонии, стрессовой нагрузки, протромбина и увеличением левого предсердия. При снижении концентрации тестостерона ухудшалось КЖ больных. Уровни депрессии и тревоги у больных с андрогенодефицитом были выше, чем у лиц с нормальным уровнем тестостерона (табл. 10).
Таблица 10.
Психовегетативный статус больных ФП с различным уровнем тестостерона.
Показатель. | Больные с андрогено-дефицитом (n=93). | Больные без андрогено-дефицита. (n=95). | Р (t-критерий). | |
Тревога, баллы. | 12,8±2,1. | 8,9±1,7. | <0,001. | |
Депрессия, баллы. | 13,2±2,0. | 9,2±2,2. | <0,001. | |
Синдром вегетативной дистонии, баллы. | 36,3±8,2. | 23,4±6,8. | <0,001. | |
Стресс-события, баллы. | 242±71. | 118±54. | <0,001. | |
Кроме того, пациенты с дефицитом тестостерона имели значительно бульшую стрессовую нагрузку в течение года до включения в исследование, а также более выраженные вегетативные расстройства по сравнению с мужчинами, у которых уровень андрогенов был нормальным.
По данным ЭхоКГ, у больных с андрогенным дефицитом размер левого предсердия (ЛП) и ИММЛЖ были больше, чем у пациентов с нормальным уровнем тестостерона (табл. 11).
У пациентов с андрогенным дефицитом среднее значение показателя КЖ было 35,54,2 балла, а у мужчин с нормальным уровнем тестостерона — 30,73,4 балла (р<0,05). Это означает, что наличие андрогенодефицитного состояния сопровождается бульшим количеством ограничений, ухудшающих КЖ.
У мужчин с андрогенным дефицитом основными причинами ухудшения КЖ были нарушения сна, проблемы в сексуальной сфере, затруднения в поездках из дома куда либо. Обратило на себя внимание значительное различие между группами по такому пункту, как затруднения в сексуальной сфере. При наличии андрогенодефицита проблемы в интимной жизни, ухудшающие КЖ, отметили 74,6% мужчин против 38,3% пациентов с нормальным уровнем тестостерона (р<0,001).
Таблица 11.
Данные эхокардиографии у больных ФП сравниваемых групп.
Показатель. | Больные с андрогено-дефицитом (n=93). | Больные без андрогено-дефицицита (n=95). | Р (t-критерий). | |
АО, мм. | 29±5. | 27±4. | >0,05. | |
ЛП, мм. | 41±3. | 33±3. | 0,003. | |
КСР ЛЖ, мм. | 43±5. | 42±4. | >0,05. | |
КДР ЛЖ, мм. | 57±4. | 55±6. | >0,05. | |
ТМЖП, мм. | 11±2. | 10±2. | >0,05. | |
ТЗСЛЖ, мм. | 10±3. | 10±2. | >0,05. | |
ИММ ЛЖ, г/м2 | 132±21. | 118±20. | 0,02. | |
Результаты коррекции андрогенного дефицита у мужчин с фибрилляцией предсердий Среди 188 мужчин, страдавших пароксизмальной формой ФП, 93 человека имели приобретенный дефицит тестостерона. Данная когорта случайным образом была поделена на основную группу (47 больных, получавших антиаритмическую терапию и ЗГТ) и группу сравнения (46 пациентов, получавших только антиаритмическое лечение). Группы были сопоставимы по возрасту, длительности заболевания, наличию сопутствующей артериальной гипертензии, ХСН.
Проведение ЗГТ в течение 6-ти месячного периода сопровождалось повышением уровня общего тестостерона, а также его свободной и биодоступной фракций (табл. 12). Снижение концентрации белка, связывающего половые стероиды (ГСПС), на фоне повышения уровня общего тестостерона привело к существенному росту индекса свободных андрогенов. Клинические проявления андрогенного дефицита, выраженные суммой баллов опросника AMS, стали значительно менее выраженными. Напротив, в группе сравнения исходные показатели андрогенного статуса не изменились.
Таблица 12.
Показатели андрогенного статуса больных ФП на 180-й день.
Показатель. | Основная группа. | Группа сравнения. | |||
Исходно. | 6 мес. | Исходно. | 6 мес. | ||
AMS, баллы. |
|
| 46,2 (37,8−49,5). |
| |
Тестостерон, нмоль/л. | 8,9. (6,1−9,8). |
|
|
| |
ГСПС, нмоль/л. |
|
|
|
| |
Тестостерон свободный, пмоль/л. |
|
|
|
| |
Тестостерон биодоступный, нмоль/л. |
|
|
|
| |
ИСА, %. | 28,6 (24,4−31,7). |
|
|
|
* - значимость различий по сравнению с основной группой р<0,01 по критерию Mann-Whitney; # - значимость различий по сравнению с исходными данными в основной группе р<0,01 по критерию Wilcoxon.
На фоне приема УТ пациенты основной группы отмечали увеличение выносливости и мышечной силы, повышение физической и умственной активности, улучшение сна, значительное уменьшение таких симптомов, как потливость, ощущение жара, сердцебиение, головные боли. К 180-му дню лечения большинство пациентов сообщили о повышение либидо, частоты ночных эрекций, способности к проведению половых актов и их частоты, возрастанию удовлетворенности от сексуальных контактов. Так, если на момент включения в исследование 79% мужчин испытывали затруднения в половой жизни, то через 6 месяцев ЗГТ — только 42% опрошенных (p<0,001).
На фоне проводимого лечения количество пароксизмов ФП статистически значимо уменьшилось. По результатам СМ ЭКГ у пациентов основной группы количество пароксизмов ФП в сутки на одного пациента снизилось с 8,78 (6,2−10,1) до 4,3 (3,09−5,12), а в группе сравнения — с 8,69 (6,41−9,96) до 6,2 (4,12−7,36) (р=0,01) по критерию Mann-Whitney). У больных, получавших УТ, уменьшение количества пароксизмов ФП произошло в 1,9 раза, а в группе сравнения — в 1,4 раза. Общая длительность пароксизмов ФП в сутки на фоне проводимой терапии также снизилась. У пациентов основной группы она уменьшилась с 68,2 (43,7−79,1) до 28,4 (21,6−38,3) мин (снижение в 2,4 раза), а в группе сравнения с 66,9 (47,1−77,4) до 41,8 (33,8−51,2) мин (снижение в 1,6 раза) (р<0,001). При анализе жалоб больных оказалось, что на фоне ЗГТ удается добиться существенного улучшения следующих расстройств: внутреннее напряжение, беспокойство, снижение работоспособности, головокружение, нарушения сна. К концу 6-го месяцев лечения у 66,7% основной группы пациентов отсутствовали клинически выраженные симптомы тревоги. Положительный эффект терапии в виде исчезновения симптомов депрессии отмечен у 82,7% мужчин, получавших УТ. Через 6 месяцев терапии было проведено контрольное Эхо-КГ исследование. Было установлено, что в основной группе произошло уменьшение размера ЛП с 40 (36−42) до 37 (34−40) мм, КДР ЛЖ — с 56 (52−59) мм до 53 (49−57), а также ИММЛЖ — с 130 (122−139) до 122 (116−129) г/м2, чего не наблюдалось в группе сравнения.
Анализ клинических эффектов ЗГТ у больных ФП с андрогенным дефицитом показал, что к концу 6-го месяца лечения в основной группе произошло статистически значимое снижение ряда антропометрических показателей, характеризующих статус ожирения — ИМТ и ОТ. Наиболее существенная положительная динамика отмечена со стороны показателей СЖТ и МЖТ/ОТ, которые уменьшились на 16,9% и 18,8% соответственно.
Суммарный показатель КЖ в основной группе статистически значимо снизился — с 35,3 (31,6−40,7) до 21,6 (18,1−25,4) баллов (р0,05), т. е. значимых различий не обнаружено.
Таким образом, применение УТ для коррекции андрогенной недостаточности у мужчин, страдающих пароксизмальной формой ФП, оказывало благоприятное влияние не только на андрогенный статус пациентов, но и на частоту и продолжительность приступов аритмии, психовегетативные расстройства, качество жизни больных. Полученные результаты свидетельствуют о полезности дальнейшего изучения гендерных подходов к лечению нарушений сердечного ритма, что согласуется с мнением других исследователей (Wolbrette D.L., 2003). При назначении УТ больным сердечно-сосудистыми заболеваниями и андрогенным дефицитом была установлена хорошая переносимость препарата в использованной дозировке. Нежелательных эффектов, которые бы требовали отмены препарата, отмечено не было. Побочные эффекты (тошнота, повышение полового возбуждения, преходящее головокружение в начале лечения) встречались менее чем в 1% случаев. Для контроля безопасности ЗГТ проводилось исследование уровня простатического специфического антигена (ПСА) всем больным до начала лечения и на 180-й день. Исходный уровень ПСА у обследованных мужчин составил 0,84 нг/мл (95% ДИ — 0,6−1,2). Через 6 месяцев ЗГТ средний уровень ПСА в крови больных был равен 1,0 нг/мл (0,7−1,23) (р>0,05). Таким образом, использование УТ в суточной дозе 80−120 мг для коррекции приобретенного андрогенного дефицита у мужчин с ССЗ не вызывает статистически значимого повышения уровня ПСА.