Кинетика растворения одиночной частицы

Возможность вычисления этого интеграла зависит от явного вида корреляционного соотношения, из которого находится зависимость fi®. Интегрирование по радиусу может производиться по интервалам в соответствии с разными режимами обтекания частицы или любыми численными методами. Существуют твердые вещества, при растворении которых выделяется газовая фаза. Кинетика такого рода процессов осложнена… Читать ещё >
Кинетика растворения одиночной частицы (реферат, курсовая, диплом, контрольная)
Рассмотрим кинетику растворения, зависящую только от скорости химического взаимодействия растворяемого вещества при постоянных значениях концентраций растворителя (ср) и температуры процесса [14]. Массу и наружную поверхность сферической частицы можно выразить через текущее значение радиуса г:
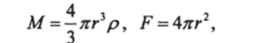
где р — плотность растворяющегося вещества.

Подставим значения массы и наружной поверхности в кинетическое уравнение скорости растворения (32.2), получим дифференциальное уравнение:
Отрицательный знак соответствует убыванию радиуса растворяющейся частицы (dr < 0).
В результате интегрирования уравнения (32.5) при начальном условии г|г=о = И) получаем линейный характер уменьшения радиуса частицы в процессе ее растворения:
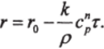
Время полного растворения частицы тт соответствует условию г = О в соотношении (32.5):
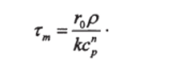

В большинстве случаев лимитирующей стадией процесса растворения является диффузионный отвод растворенного вещества от поверхности растворения (зависимость 32.1). Кинетическое уравнение (32.1) записывается относительно радиуса сферической частицы. Переменные гит разделяются при любом виде зависимости коэффициента массоотдачи Р (г) от радиуса частицы:
где Ас = (с*- с) — движущая сила (постоянная величина по условию задачи).
Связь между временем т от начала растворения до текущего значения т и значением текущего радиуса г от начального го до текущего значения радиуса растворяющейся частицы устанавливается интегрированием уравнения (32.6).
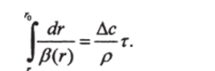
Возможность вычисления этого интеграла зависит от явного вида корреляционного соотношения, из которого находится зависимость fi®. Интегрирование по радиусу может производиться по интервалам в соответствии с разными режимами обтекания частицы или любыми численными методами.
Существуют твердые вещества, при растворении которых выделяется газовая фаза. Кинетика такого рода процессов осложнена дополнительным влиянием на скорость растворения большого количества мелких пузырьков газа, образующихся у поверхности растворения.
Растворение твердых веществ обычно сопровождается выделением теплоты растворения, что, в принципе, должно влиять на интенсивность внешней массоотдачи и на величину концентрации насыщения с*. Однако температура поверхности растворения, где и происходит выделение теплоты, максимально повышается не более чем на несколько градусов, что объясняется высокой теплоемкостью жидких растворителей по сравнению с медленно выделяющейся теплотой растворения. По этой причине процессы растворения обычно рассматриваются как изотермические.