Примеры решения задач

Решение. Пусть имеется JV, молекул первого сорта и N2 молекул второго сорта. Тогда число перестановок одинаковых молекул равно N{N2. Элементарный фазовый объем системы равен. Где dm — масса частиц, координаты которых лежат в интервале от z до z + dz. Используя распределение Больцмана, получим (5- площадь поперечного сечения столба газа): Решение. Имеем: cr -cv = R cP/cv = у. Отсюда cv — R/(у -1… Читать ещё >
Примеры решения задач (реферат, курсовая, диплом, контрольная)
1. Найти центр масс столба идеальною газа в однородном ноле тяготения, если ускорение свободною падения равно g, масса молекулы газа т, температура газа Т.
Решение. Согласно распределению Больцмана, концентрация молекул в столбе газа зависит только от расстояния, отсчитанного от нулевого уровня потенциальной энергии. Поэтому центр масс лежит на оси симметрии столба, на расстоянии zc от его основания. По определению центра масс:
Поскольку число частиц в газе велико, их распределение можно считать непрерывным и перейти от суммирования к интегрированию, тогда:
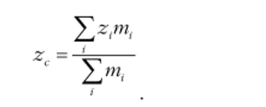
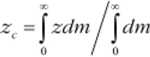
где dm — масса частиц, координаты которых лежат в интервале от z до z + dz. Используя распределение Больцмана, получим (5- площадь поперечного сечения столба газа):
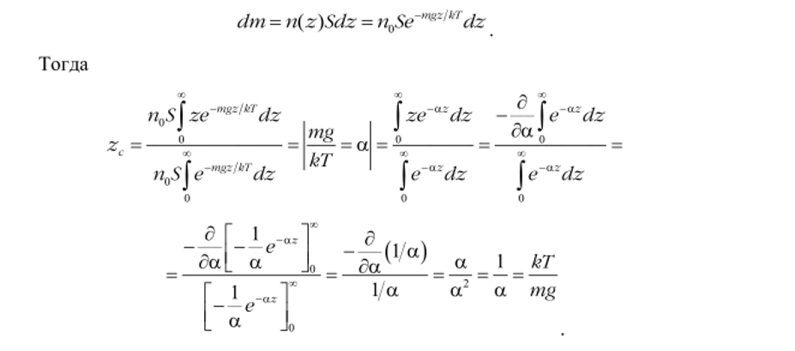
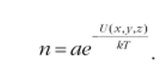
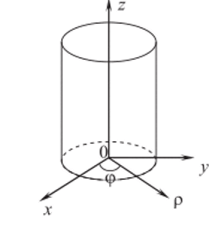
В силу симметрии задачи удобно воспользоваться цилиндрической системой координат р, ер, z (см. рис. 13), которая вращается вместе с цилиндром. В отсутствии вращения потенциальная энергия молекул газа равна mgz. Во вращающейся же системе координат на молекулы действует дополнительно центробежная сила инерции Fc =wcop. По общим правилам механики Fc—dUjф, и ей соответствует потенциальная энергия.
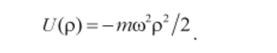
л.
Рис. 13
Следовательно, полная потенциальная энергия молекул газа равна: U(р, ф, z) = mgz — wcop /2.
Тогда распределение Больцмана принимает вид:
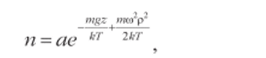
где постоянная определяется условием нормировки: J ndV = N. Под;
V
ставляя сюда предыдущее выражение и вводя обозначения: а = mgfkT, р = тт/21гТ, получим:
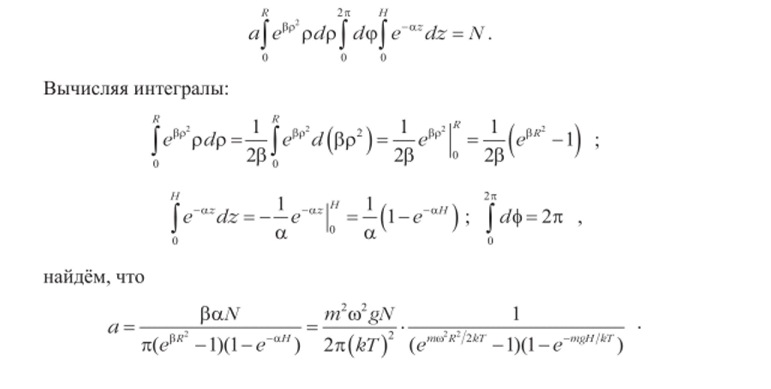

4. Вывести закон Дальтона для смеси двух идеальных газов.
Решение. Пусть имеется JV, молекул первого сорта и N2 молекул второго сорта. Тогда число перестановок одинаковых молекул равно N{N2. Элементарный фазовый объем системы равен.
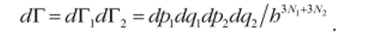
Отсюда ясно, что интеграл состояний смеси равен произведению интегралов состояний компонент: Z = Z. Z, при этом, например ,.
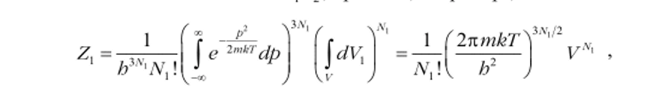
где V — объем всей смеси (поскольку координаты молекул меняются в пределах области, занимаемой всем газом).
Тогда, свободная энергия смеси 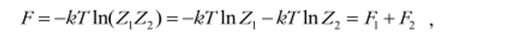 а давление равно.
а давление равно.
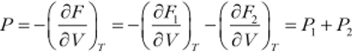
где Р} и Рг — парциальные давления компонент, то есть, давления, вычисленные в предположении, что каждая компонента занимает весь объем смеси.
5. Молярная теплоёмкость идеального газа в некотором процессе изменяется по закону с = а/Г, где, а — некоторая постоянная. Показатель адиабаты (аза равен у. Найти уравнение процесса в параметрах Я, V. Вычислить работу, которую совершает в этом процессе один моль (аза при ею нагревании от температу ры Ти до температуры в г) раз большей.
Решение. Имеем: cr -cv = R cP/cv = у. Отсюда cv — R/(у -1). Запишем первое начало термодинамики dE = dQ—PdV и уЧТём, что для одного моля газа dE = cvclT, a dQ — cdT. Тогда: cvdT — cdTPdV.[1]

- 6. Найти теплоёмкость системы, состоящей из N независимых двумерных гармонических осцилляторов с энергетическим спектром E)t=hv (n+1), где «= 0,1,2,… Каждый энергетический уровень
- (п +1) -кратно вырожден.
Решение. Аналогично тому, как это было сделано в § 7, запишем, прежде всего, выражение для статистической суммы:


а из первого и критическое давление 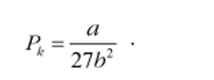
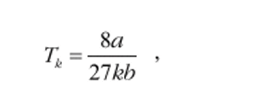
- [1] Вычисления полностью аналогичны тем, которые проделаны в § 3.