Карбокатионы (карбониевые ионы)

Карбокатион — заряженная частица, имеющая вакантную р-орбиталь на атоме углерода, находящегося во втором валентном состоянии (5'р2-гибридизация). Плоская структура такой частицы однозначно подтверждена экспериментально (рис. 10). В последнем случае происходит перестройка углеродного скелета молекулы — явление, весьма распространённое в органической химии. Движущей силой таких перегруппировок… Читать ещё >
Карбокатионы (карбониевые ионы) (реферат, курсовая, диплом, контрольная)
Карбокатионы — координационно ненасыщенные молекулярные частицы, несущие единичный положительный заряд на атомах углерода. Карбокатионы — группы атомов, содержащих атом углерода с шестью электронами.
Карбокатионы образуются или путём гетеролитического разрыва поляной связи С —> X:
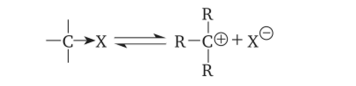
или путем присоединения положительно заряженной частицы (протона, катиона) по кратной связи:
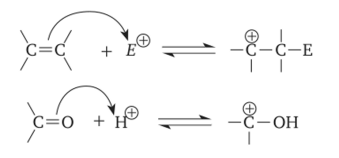
Карбокатион — заряженная частица, имеющая вакантную р-орбиталь на атоме углерода, находящегося во втором валентном состоянии (5'р2-гибридизация). Плоская структура такой частицы однозначно подтверждена экспериментально (рис. 10).
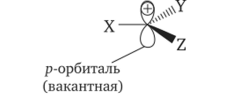
Рис. 10. Атомно-орбитальная модель карбокатиона XYZC+
Атомно-орбитальная модель карбокатиона демонстрирует, что три 5р2-гибридные орбитали образуют ковалентные связи с заместителями X, Y и Z у карбокатионного центра. Вакантная р-орбиталь располагается перпендикулярно плоскости трёх о-связей.
Лёгкость образования карбокатионов растёт в ряду:
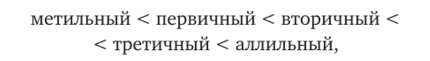
т.е. соблюдается та же закономерность, что и для свободных радикалов. Относительную стабильность карбокатионов объясняют степенью делокализации положительного заряда. Донорные алкильные группы у карбокатионного центра за счёт +7-эффекта частично снижают величину положительного заряда (снижают степень его локализации на конкретном атоме углерода).
Высокая стабильность (соответственно и лёгкость образования) аллилкарбокатиона объясняется ролью мезомерного эффекта (сопряжение электронов я-связи с вакантной р-орбиталью карбокатионного центра), в результате которого достигается высокая степень делокализации заряда в мезомерном карбокатионе:
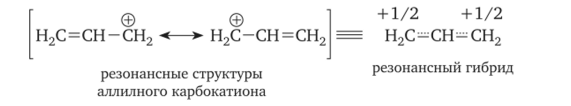
Аналогичным образом достигается стабилизация карбокатиона, если рядом с карбокатионным центром находятся гетероатомы с неподелёнными электронными парами, например, стабилизация метоксиметильного карбокатиона:
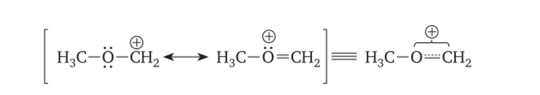
В карбокатионе положительно заряженный атом углерода представляет собой чрезвычайно активный электрофильный центр, который способен образовывать новую ковалентную связь за счёт своей вакантной орбитали. Это происходит при взаимодействии с любым нуклеофильным реагентом (Nu), который предоставляет для этого свою электронную пару:
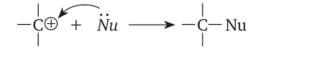
Другим распространённым направлением превращений карбокатионов является их депротонирование с образованием алкенов:
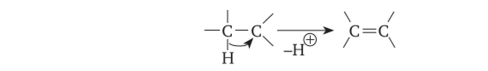
Одно из обобщений в химии карбокатионов (особый признак реакций, протекающих с их участием) состоит в том, что ионы карбонил могут перегруппировываться с образованием более устойчивого карбониевого иона. Суть перегруппировки: к углероду, несущему положительный заряд, мигрирует атом водорода или алкильная группа с парой электронов от соседнего атома углерода. Углерод, от которого уходит эта группа, приобретает положительный заряд (перенос карбокатионного центра). Миграция водорода с парой электронов известна как гибридный сдвиг.
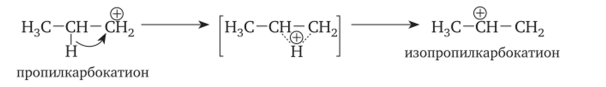
Аналогичная миграция алкильной группы известна как алкильный сдвиг.
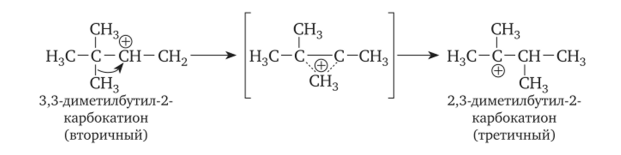
В последнем случае происходит перестройка углеродного скелета молекулы — явление, весьма распространённое в органической химии. Движущей силой таких перегруппировок является понижение свободной энергии активной частицы.
Участие карбокатионов как промежуточных активных частиц обсуждается в механизмах различных реакций органической химии, в том числе химии алкенов, спиртов, алкилгалогенидов и многих других классов органических соединений.