Качественные реакции.
Характеристика производных антрацена

Реакция с ацетатом магния Реакция основана на способности антраценпроизводных образовывать окрашенные комплексы с ацетатом магния; при этом 1,2-диоксипроизводные образуют фиолетовое окрашивание; 1,4 — пурпуровое;1,6- и 1,8 — оранжево-красное. После окончания хроматографирования пластинку вынимали из камеры, отмечают линию финиша пробега растворителя, высушивали и просматривают в видимом и УФ… Читать ещё >
Качественные реакции. Характеристика производных антрацена (реферат, курсовая, диплом, контрольная)
1. Реакция образования антрахинолятов со щелочью.
Проба может проводиться в трех вариантах:
- а) на сухом сырье — при нанесении нескольких капель 5−10% раствора натрия гидроксида на сырье появляется вишнево-красное пятно.
- б) с водным извлечением (1:10) — при добавлении к водному извлечению из сырья нескольких капель 5−10% раствора щелочи, цвет становится красным.
- в) реакция Борнтрегера. Позволяет обнаружить эмодины в присутствии других производных антрацена.
Методика проведения реакции.
- 1. 0,2 г измельченного сырья кипятят в течение 2 мин с 5 мл 10%едкого натра. После остывания смесь разбавляют 5мл воды и фильтруют.
- 2. 3 мл фильтрата помещают в делительную воронку, добавляют 3 мл10% соляной кислоты и 10 мл хлороформа.
- 3. Осторожно перемешивают и после расслоения жидкости сливают хлороформный слой, фильтруя его через небольшой комочек ваты.
- 4. Фильтрат встряхивают с 10 мл 10% раствора аммиака и наблюдают появившееся окрашивание.
При наличии 1,8-диоксиантрахинонов аммиачный слой принимает вишнево-красное окрашивание, 1. 4- -диоксиантрахинонов — пурпурное окрашивание, 1. 2-диоксиантрахинонов — фиолетовое окрашивание.
Сущность реакции заключается в следующем: при кипячении растительного материала со щелочью происходит гидролизантрагликозидов с образованием свободных агликонов. Одновременно антрони антранолпроизводные окисляются до антрахинонов. Образовавшиеся оксиантрахиноны за счет фенольных гидроксилов дают феноляты (антрахиноляты), растворимые в воде. При подкислении водно-щелочного раствора диссоциация фенольных гидроксилов подавляется, и соединения становятся липофильными, в результате чего при встряхивании с хлороформом они из водного слоя переходят в хлороформный, хлороформный слой при этом принимает желтую окраску оксиантрахинонов. При встряхивании хлороформного слоя с раствором аммиака вновь происходит образование фенолятов окрашивающих аммиачный слой. Феноляты оксиантрахинонов имеют яркий вишнево-красный, пурпурный или фиолетовый цвет в зависимости от положения оксигрупп.
Написать уравнения реакций.
2. Реакция с ацетатом магния Реакция основана на способности антраценпроизводных образовывать окрашенные комплексы с ацетатом магния; при этом 1,2-диоксипроизводные образуют фиолетовое окрашивание; 1,4 — пурпуровое;1,6- и 1,8 — оранжево-красное.
Методика проведения реакции.
- А). 1,0 г измельченного сырья поместили в колбу объемом 50 мл со шлифом, добавьте 10 мл 95% этилового спирта и нагрели на водяной бане с обратным холодильником 10 минут. Охладили полученное извлечение.
- Б). К 1 мл 1% спиртового раствора ацетата магния прибавили несколько капель извлечения из сырья
- 3. Сублимация антраценпроизводных
Сущность реакции: содержащиеся в растительном материале антрагликозиды при высокой температуре расщепляются с образованием свободных агликонов; одновременно производные антрона и антронола окисляются до антрахинонов, которые возгоняются.
Методика проведения реакции Поместили на дно сухой пробирки небольшое количество измельченного сырья и, осторожно нагрели, держа пробирку почти горизонтально. В результате сублимат конденсировался на холодных участках пробирки в виде желтых капель или желтых игольчатых кристаллов. После охлаждения пробирки к сублимату прибавили 1 каплю 5%NaOH в этиловом спирте; появляется яркое красное или фиолетовое окрашивание в зависимости от состава антраценпроизводных.
- 3. Хроматографическое определение антраценпроизводных в растительном сырье.
- 1). 0,3 г измельченного растительного сырья нагревали с 3 мл этилового спирта в течение 5 мин, доводя до слабого кипения. После остывания фильтровали.
- 2). 0,1 мл извлечения наносят на линию старта и хроматографируют в системе «этилацетат: метиловый (этиловый) спирт: вода», взятых в соотношениях 100:17:13, на пластинках «Силуфол». (Одновременно хроматографируют стандарт «свидетель», нанося его раствор рядом с исследуемым извлечением).
- 3). После окончания хроматографирования пластинку вынимали из камеры, отмечают линию финиша пробега растворителя, высушивали и просматривают в видимом и УФ свете до и после проявления парами аммиака или 5% NaOH в этиловом спирте.
- 4. Превращение антрапроизводных в коре крушины ломкой при хранении или прогревании при 100 °C.
В первичной коре крушины содержится первичный гликозидфрангуларозид, который проявляет рвотное действие. Антранолы являются мобильными соединениями и способны к окислению даже кислородом воздуха. Поэтому кору крушины применяют или после годичного хранения или процесс окисления франгулоразида ускоряют нагреванием при 100 °C в течение 1 часа. В итоге франгуларозид превращается в 11глюкофрангулин. Далее при ферментативном гидролизе отглюкофрангулина отщепляется глюкоза, биозид превращается в монозидфрангулин. В дальнейшем франгулин расщепляется на франгула-эмодинирамнозу. Таким образом, в коре крушины, готовой к медицинскому применению, могут одновременно находиться глюкофрангулин, франгулин, франгула-эмодин.
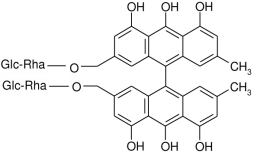
франгуларозид глюкофрангулин франгулин франгула-эмодин.