Элементы группы VIIB

Шсстивалснгный марганец известен главным образом в виде солей неустойчивой марганцовистой кислоты — манганатов: К2Мп04 и др. В твердом состоянии это почти черные вещества с зеленоватым отливом, их водные растворы зеленые. Их устойчивость повышается в присутствии щелочи. Оксид Мп03 — летучее вещество, образующее пурпурно-красные пары и отщепляющее кислород уже при 50 °C. Поэтому при термическом… Читать ещё >
Элементы группы VIIB (реферат, курсовая, диплом, контрольная)
Группа VIIB состоит из четырех (/-элементов с нечетными атомными номерами: марганец 25МП, технеций 43Тс, рений 75Re и борий 107Bh (табл. 27.10). Борий назван в честь великого датского физика Н. Бора, создавшего первую квантовую теорию электронного строения атома. Первоначально название нильсборий предлагалось дать элементу № 105.
Таблица 27.10
Характеристика элементов группы VIIB
Свойство. | Элемент. | ||
25 М'1 | «Тс. | 75Ке | |
Радиус г атома (ковалентный), пм. | |||
Содержание в земной коре. (О, %. | 0,095. | 4−10-«. | |
Содержание в организме человека со, %. | 6,6−10. | — | — |
Электроотрицательность х | 1,6. | 1,9. | 1,9. |
Главные СО | +2, +3, +4, +6, +7. | +4, +5, +6, +7. | +3, +4, +6, +7. |
* Биогенный элемент.
Марганец в природе представляет собой одиночный нуклид ^|Мп. Марганец был открыт в 1774 г. Ю. Ганом (Швеция).Технеций не имеет стабильных изотопов, но его радиоактивные изотопы нарабатываются в ядерных реакторах в количествах, исчисляемых тоннами. Самый долгоживущий — изотоп ^|Тс с периодом полураспада 6,6−106 лет. Технеций открыт в 1937 г. К. Перье и Э. Сегре (Италия). Рений — очень редкий элемент, открытый последним из природных химических элементов в 1925 г. (В. Ноддак, И. Таке и О. Берг, Германия). В природе есть один стабильный нуклид (^|Re, 37,4%) и один долгоживущий радионуклидRe (62,6%, Г½ = 4,2−1010 лет).
Распространенность марганца в природе достаточно высокая (см. табл. 27.10). Важнейшая марганцевая руда — пиролюзит Мп02. Имеют промышленное значение также минералы хаусманит Мп304 и браунит Мп203. Рений минералов не имеет. Основным источником его получения являются отходящие газы при выплавке молибдена. Минерал MoS2 может содержать десятитысячные доли процента рения. Мировое производство рения составляет около 20 т/год. Производство технеция, выделяемого из продуктов распада урана в реакторах, превышает 1 т/год.
Марганец близок по внешнему виду к железу. Технеций и рений — серебристо-белые металлы. Некоторые физические свойства металлов приведены в табл. 27.11. Это тугоплавкие металлы, причем рений, но тугоплавкости уступает только вольфраму.
Таблица 27.11
Физические свойства металлов группы VIIB.
Свойство. | Металл. | ||
марганец. | технеций. | рений. | |
Плотность, г/см3 | 7,3. | и. | 20,8. |
?, 1Л> С. | |||
^КНП" ^. | |||
Электрическое сопротивление, Ом м (при 273 К). | 143−10 8 | 22,6−10 8 | 17,2 -10 8 |
Марганец важен как металл, применяемый в черной металлургии для раскисления, десульфурирования и легирования сталей. Для этих целей используется более 90% добываемого марганца. Общая добыча марганца составляет до 20 млн т. Материалы, содержащие марганец, применяются в радиотехнических устройствах, для получения окрашенного стекла, в медицине. Сплав манганин (83% Си, 13% Мп и 4% Ni) применяется в электрических сопротивлениях, так как его удельное сопротивление почти не зависит от температуры.
Соединения технеция применяются в медицине для диагностики опухолевых заболеваний. Большая часть добываемого рения используется в платино-рениевых катализаторах в нефтяной промышленности для повышения качества моторного топлива. Сплавы рения применяются для изготовления электрических контактов, для покрытия других сплавов, применяемых в электротехнике.
Марганец — биогенный микроэлемент. Ионы Мп2+ активируют значительное число ферментов. В составе некоторых ферментов марганец содержится постоянно. В организме человека в среднем имеется около 12 мг марганца. Он также является необходимым элементом в фотосинтезирующей системе растений. При недостатке марганца у растений нарушается синтез хлорофилла. Соединения марганца включаются в состав микроудобрений.
Металлический марганец химически активен и по свойствам ближе к железу, чем к хрому. Стандартный редокс-потенциал марганца отрицателен: ф°(Мп2+/Мп) = -1,19 В. С разбавленными кислотами марганец реагирует с выделением водорода. Концентрированная серная кислота восстанавливается до S02. Сам марганец окисляется до Мп2+:
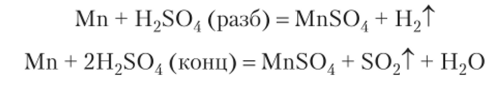
Хлор, бром и галогеноводородные кислоты также окисляют марганец до двухвалентного состояния. С серой марганец образует MnS и MnS2 (при избытке серы).
В нейтральных водных растворах двухвалентный марганец устойчив. Гидратированный ион Мп2+ имеет бледно-розовую окраску, почти не заметную в растворе, но кристаллогидраты солей розовые.
Гидроксид Мп (ОН)2 белого цвета, имеет основные свойства, выпадает в осадок в щелочной среде и постепенно окисляется кислородом до Мп (ОН)3. При этом осадок темнеет.
Ион Мп3+ в водном растворе неустойчив и диспропорционирует:
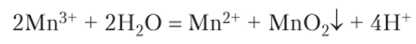
На самом деле бурый осадок Мп02 содержит переменное количество воды: Мп02-хН20. Кристаллогидраты солей трехвалентного марганца не существуют. Но известно много комплексных соединений Мп (Ш): К3|Мп (С204)3| пурпурно-красного цвета, K3|Mn (CN)6| темно-красного цвета и др.
Четырехвалентный марганец образует относительно немного химических соединений, но среди них есть очень устойчивый оксид Мп02, вещество черного цвета (в гидратированной форме бурый). Он образуется во многих реакциях как при окислении Мп (П), так и при восстановлении Mn (VII):
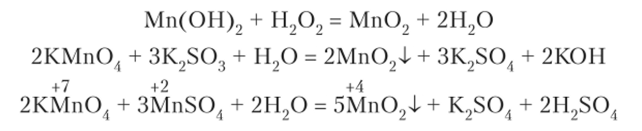
В кислой среде Мп02 окислитель, а в щелочной — восстановитель:
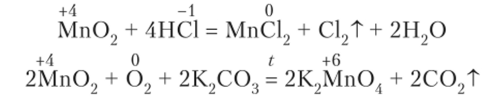
Оксид марганца (1У) ускоряет реакции разложения различных неустойчивых веществ — перекиси водорода, хлората калия и др.
Пятивалентное состояние для марганца нехарактерно, известны лишь немногие соединения, например K[MnF6j.
Шсстивалснгный марганец известен главным образом в виде солей неустойчивой марганцовистой кислоты — манганатов: К2Мп04 и др. В твердом состоянии это почти черные вещества с зеленоватым отливом, их водные растворы зеленые. Их устойчивость повышается в присутствии щелочи. Оксид Мп03 — летучее вещество, образующее пурпурно-красные пары и отщепляющее кислород уже при 50 °C. Поэтому при термическом разложении перманганата калия образуются К2Мп04 и оксид Мп02 вместо неустойчивого МпОэ:
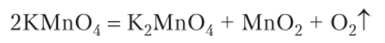
Если разложение проводится в присутствии вещества, служащего источником оксида калия, то весь марганец переходит в манганат:
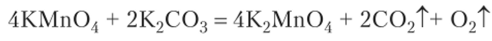
Среди соединений марганца важное практическое значение имеет перманганат калия, уже неоднократно упоминавшийся в этом учебнике в связи с его окислительными свойствами. Перманганат калия образуется при диспропорционировании манганата калия или при его окислении в процессе электролиза:
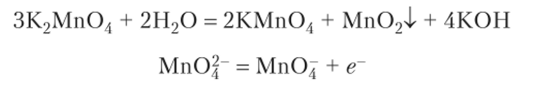
Водные растворы КМп04 в темноте устойчивы, но на свету происходит разложение с образованием бурого осадка Мп02:
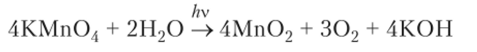
Перманганат калия применяется в медицине для промывания кожных покровов и слизистых при ранениях и заболеваниях, а также для полоскания. Антисептическое действие основано на окислительных свойствах. Перманганат калия применяется также в аналитической химии для количественного определения восстановителей, а при специальных методах титрования — и для определения окислителей.
Оксид марганца (УП) образуется в виде темно-зеленой жидкости при действии концентрированной серной кислоты на кристаллы перманганата калия:
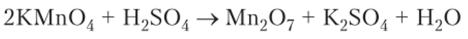
Это кислотный оксид, образующий с водой сильную марганцевую кислоту НМп04. При температуре выше 0 °C оксид марганца (УП) может разлагаться со взрывом:
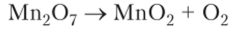
Тяжелые элементы группы VIIВ технеций и рений в высшей степени окисления более устойчивы, чем марганец. Окислительные свойства пертехнатов и перренатов значительно слабее, чем перманганатов. Эта же закономерность наблюдалась в группах IVB — VIВ.