Алкены.
Органическая химия

Помимо изомерии углеродного скелета, в ряду алкенов появляется еще и изомерия положения двойной связи. В общем виде изомерия такого типа — изомерия положения заместителя (функции) — наблюдается во всех случаях, когда в молекуле имеются какие-либо функциональные группы. Для алкана С4Н10 возможны два структурных изомера: Углеводородные радикалы, образованные из алкенов, получают суффикс —енил… Читать ещё >
Алкены. Органическая химия (реферат, курсовая, диплом, контрольная)
Углеводороды, в молекуле которых помимо простых а-связей углерод — углерод и углерод — водород имеются углерод-углеродные я-связи (см. гл. 1), называются непредельными. Так как образование я-связи формально эквивалентно потерю молекулой двух атомов водорода, то непредельные углеводороды содержат на 2п атомов водорода меньше, чем предельные, где п — число я-связей:
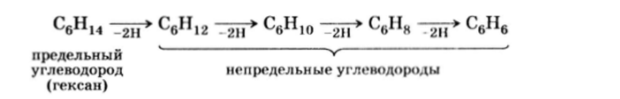
Ряд, члены которого отличаются друг от друга на (2Н)Л, называется изологическим рядом. Так, в приведенной выше схеме изологами являются гексаны, гексены, гексадиены, гексины, гексатриены и т. д.
Углеводороды, содержащие одну я-связь (т. е. двойную связь), называются алкенами (олефинами) или, по первому члену ряда — этилену, этиленовыми углеводородами. Общая формула их гомологического ряда СлН2л.
Номенклатура
В соответствии с правилами ИЮ11АК при построении названий алкенов наиболее длинная углеродная цепь, содержащая двойную связь, получает название соответствующего алкана, в котором окончание -ан заменено на —ен. Эта цепь нумеруется таким образом, чтобы углеродные атомы, участвующие в образовании двойной связи, получили номера, наименьшие из возможных:
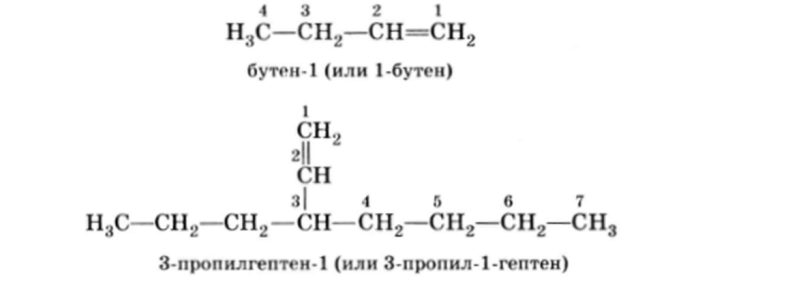
Радикалы называются и нумеруются как и в случае алканов.
Для алкенов сравнительно простого строения разрешается применять более простые названия. Так, некоторые наиболее часто встречающиеся алкены называют, добавляя суффикс -ен к названию углеводородного радикала с тем же углеродным скелетом:
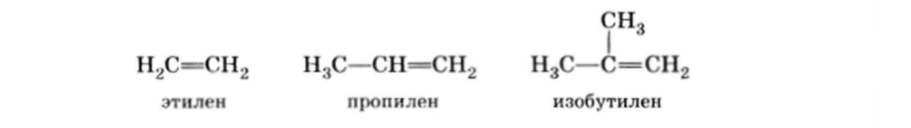
Углеводородные радикалы, образованные из алкенов, получают суффикс —енил. Нумерация в радикале начинается от углеродного атома, имеющего свободную валентность. Однако для простейших алкенильных радикалов вместо систематических названий разрешается использовать тривиальные:

Водородные атомы, непосредственно связанные с ненасыщенными атомами углерода, образующими двойную связь, часто называют винильными атомами водорода.
Изомерия
Помимо изомерии углеродного скелета, в ряду алкенов появляется еще и изомерия положения двойной связи. В общем виде изомерия такого типа — изомерия положения заместителя (функции) — наблюдается во всех случаях, когда в молекуле имеются какие-либо функциональные группы. Для алкана С4Н10 возможны два структурных изомера:
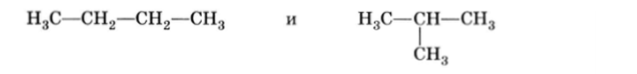
Для алкена С4Н8 (бутена) возможны три изомера:
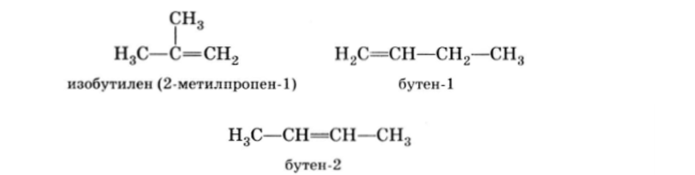
Бутен-1 и бутен-2 являются изомерами положения функции (в данном случае ее роль выполняет двойная связь).
Еще один вид изомерии, появляющийся у соединений, содержащих двойную связь, будет рассмотрен в конце главы.
Строение ДВОЙНОЙ связи. Электронное строение л-связи было рассмотрено в гл. 1. Дополнительно следует указать на следующее. Энергия разрыва молекулы по двойной связи С=С равна 611 кДж/моль; так как энергия о-связи С—С равна 339 кДж/моль, то энергия разрыва л-связи равна лишь 611 -339 = 272 кДж/моль. л-Электроны значительно легче о-электронов поддаются влиянию, например, поляризующих растворителей или воздействию любых атакующих реагентов (см. гл. 2). Это объясняется различием в симметрии распределения электронного облака аи л-электронов. Максимальное перекрывание р-орбиталей и, следовательно, минимальная свободная энергия молекулы реализуются лишь при плоском строении винильного фрагмента и при укороченном расстоянии С=С, равном 0,134 нм, т. е. значительно меньшем, чем расстояние между углеродными атомами, связанными простой связью (0,154 нм). С поворотом «половинок» молекулы относительно друг друга по оси двойной связи степень перекрывания орбиталей снижается, что связано с затратой энергии. Следствием этого является отсутствие свободного вращения по оси двойной связи и существование геометрических изомеров при соответствующем замещении у атомов углерода (см. далее разд. 8).