Анализ строения молекулы аллилацетата

Реагенты и продукты изучаемой реакции имеют неполярные (С — С, С = С) и полярные (С — Н, С — О, С = О) ковалентные связи, возникающие в результате обобщения не спаренных валентных электронов с противоположными спинами. Зная число электронов во внешней оболочке атомов для любого органического и неорганического соединения легко написать октетные формулы. В них учитываются только внешние электроны… Читать ещё >
Анализ строения молекулы аллилацетата (реферат, курсовая, диплом, контрольная)
Аллилацетат с бруттоформулой С5Н8О2 является сложным эфиром, образованным аллиловым спиртом и уксусной кислотой:
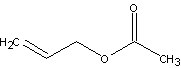
Физико-химические свойства. C5H8O2
М.м. 100,12.
Ткип 103,5−104,5°,.
Твсп 6є;
d420 0,9277; nD20 1,4040.
Растворимость в воде 3%,.
Растворяется в бензоле, смешивается с этанолом и эфиром.
Получение. Взаимодействием уксусной кислоты с пропиленом при окислении.
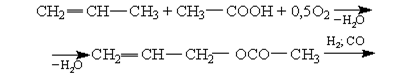
Применение. Растворитель в лакокрасочной промышленности.
Химическое поведение, реакционная способность молекулы зависит от природы составляющих ее атомов и от их взаимного расположения. Образуя молекулы, атомы изменяют свое состояние, влияют друг на друга. Наиболее сильно взаимодействуют между собой атомы, образующие химические связи.
Реагенты и продукты изучаемой реакции имеют неполярные (С — С, С = С) и полярные (С — Н, С — О, С = О) ковалентные связи, возникающие в результате обобщения не спаренных валентных электронов с противоположными спинами. Зная число электронов во внешней оболочке атомов для любого органического и неорганического соединения легко написать октетные формулы. В них учитываются только внешние электроны атомов, как образующих так и не образующих химические связи.
Электронное строение аллилцетата.
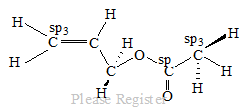
Строение аллилацетата как сложного эфира может быть представлено двумя резонансными структурами:

Эфирная группировка планарна или близка к планарной: простая связь С — О (структура I) имеет конформацию с цисоидным расположением карбонильной двойной связи и связи О — R.
Длина связи С = О 0,119−0,122 нм, связи С — О 0,131−0,136 нм, углы ОСО 122−126°, СОС 113−118°.
Кислород является более электроотрицательным элементом, по сравнению с углеродом, и поэтому электронная плотность смещена в сторону кислорода.
Карбонильная группа в молекуле аллилацетата отдалена от двойной связи, поэтому в данном соединении не наблюдается сопряжения связи с заместителем и поляризующее влияние на его р — связь проявляется в значительно меньшей степени, чем, например, в молекулах винильных соединений. Эти особенности химического строения аллилацетата обуславливают его малую реакционную способность в процессах полимеризации. Еще менее активен его радикал.