Уравнение состояния идеального газа

Найденные равенства позволяют получить ещё одно важное для приложений соотношение. Рассмотрим процесс адиабатического расширения газа, то есть расширения настолько медленного, что в любой момент времени газ можно считать находящимся в соЕго называют уравнением Пуассона. Есть и другая возможность осуществления адиабатического процесса: наоборот, проводить его настолько быстро, чтобы система… Читать ещё >
Уравнение состояния идеального газа (реферат, курсовая, диплом, контрольная)
Соотношение (4.22), которое связывает основные термодинамические характеристики газа, называется уравнением состояния идеального газа.
Это уравнение можно записать в более привычной форме, если учесть, что 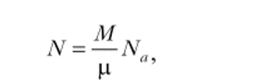
где Na = 6,023* 1023 моль~] — число молекул в одном моле газа (число Авогадро).
Тогда 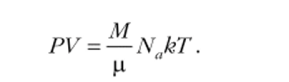
Введем еще одну постоянную.

которую называют универсальной газовой постоянной. Тогда.

Уравнение (4.23) -уравнение Клапейрона-Менделеева.
После того как определены термодинамические функции идеального газа, мы можем найти и его теплоёмкость. Для этого воспользуемся найденными в § 7 главы II соотношениями.
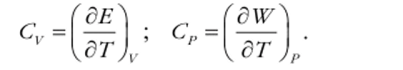
Согласно результатам предыдущего параграфа, внутренняя энергия идеального газа равна 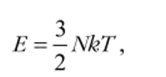 следовательно,.
следовательно,.

Последнее выражение называют соотношением Майера.
Необходимо подчеркнуть, что все полученные выражения справедливы лишь в том случае, когда рассматривается идеальный газ, молекулы которого не имеют внутренней структуры.
Найденные равенства позволяют получить ещё одно важное для приложений соотношение. Рассмотрим процесс адиабатического расширения газа, то есть расширения настолько медленного, что в любой момент времени газ можно считать находящимся в соЕго называют уравнением Пуассона.

Есть и другая возможность осуществления адиабатического процесса: наоборот, проводить его настолько быстро, чтобы система не успела обменяться теплотой с окружающей средой. В этом случае (IQ = 0, а так как dO = TdS, то и dS = 0, то есть энтропия сохраняет постоянное значение.